Până la ora actuală, nu este clar cum se declanşează scleroza laterală amiotrofică (SLA). Nu există niciun tratament eficient, iar această afecţiune care evoluează rapid este terminală. De aceea, o recentă descoperire în legătură cu proteine nefuncţionale într-un nou studiu este importantă pentru oamenii de ştiinţă.
SLA, cunoscută şi drept boala Lou Gehrig, după numele unui celebru jucător american de baseball care a suferit de această afecţiune, este o boală degenerativă a neuronilor motori care implică moartea treptată a acestor celule care controlează muşchii şi mişcările.
Cercetări anterioare au descoperit că variantele genetice asociate cu SLA pot produce aceste proteine care provoacă stres celular, cauza exactă a daunelor nu a fost încă identificată.
Un indiciu ar putea fi legăturile dintre proteinele bogate într-un aminoacid specific şi stresul dintr-un organit numit nucleolă din celulele pacienţilor cu SLA.
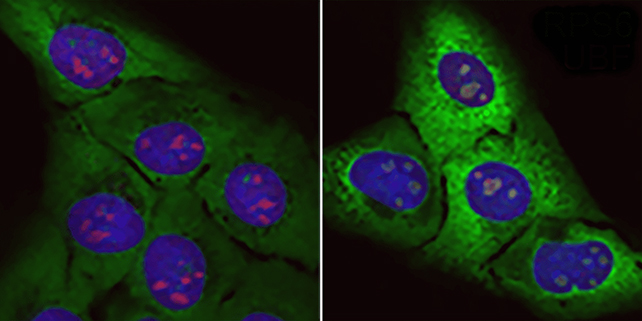
Scanare celulară. Imaginea din dreapta arată efectele proteinei toxice bogate în arginină, asupra proteinelor ribozomiale, în verde, şi a nucleolelor, în roşu. (CNIO)
O echipă condusă de cercetători de la Centrul Naţional Spaniol de Cercetare a Cancerului (CNIO) a folosit teste pe culturi de celule şi pe celule de şoarece pentru a cerceta în continuare asocierea dintre acumularea de proteine nefuncţionale şi daunele celulare în SLA.
„În cercetarea noastră, raportăm un nou model care explică modul în care stresul nucleolar induce toxicitatea în celulele animale şi aducem dovezi directe că acesta accelerează îmbătrânirea celulelor la mamifere", spune Vanesa Lafarga, specialist în biologie molecular la CNIO.
Cercetătorii au urmat un traseu biologic complex, pornind de la un lucru pe care îl ştiau deja despre SLA ereditară: aceasta se caracterizează printr-o abundenţă de peptide toxice (fragmente chimice) bogate în aminoacidul arginină.
Investigaţia a făcut legătura între această abundenţă dăunătoare şi o perturbare a capacităţii celulei de a fabrica proteine cheie de care organismul are nevoie pentru a funcţiona. Pe măsură ce procesul de fabricaţie se întrerupe, proteinele „nedorite" - care nu au nicio treabă de făcut - se acumulează.
Maşinăriile biologice de fabricaţie implicate se numesc ribozomi şi există o legătură importantă cu un alt grup de boli rare, numite ribosomopatii, în care se întâmplă ceva similar. Cunoscând că aceste boli au unele caracteristici comune cu SLA, cercetătorii speră să afle informaţii noi, care să-i ajute să înţeleagă mai bine această boală devastatoare, potenţial mortală.
Această cercetare a arătat că efectele dăunătoare ale acestor proteine nedorite - în ceea ce priveşte comunicarea şi repararea celulelor, de exemplu - se potrivesc bine cu ceea ce a fost observat anterior în cazul SLA.
„Aceste proteine sfârşesc prin a prăbuşi sistemele de mentenanţă celulară, ceea ce duce în cele din urmă la moartea neuronilor motori", spune Óscar Fernández-Capetillo, specialist în biologie molecular şi director adjunct la CNIO.
Cercetătorii sunt încă în stadii incipiente aici, deoarece aceste conexiuni au fost descoperite abia acum.
Cu toate acestea, noile cunoştinţe ar putea fi folosite mai departe pentru a aborda cauzele profunde ale unor afecţiuni precum SLA.
Deoarece stresul nucleolar declanşează, de asemenea, anumite modificări care indică o îmbătrânire biologică accelerată, sau viteza cu care celulele dau semne de uzură şi, în cele din urmă, mor, descoperirea ar putea avea aplicaţii dincolo de tratamentul pentru scleroza laterală amiotrofică.
„Abia facme primii paşi pentru a vedea dacă putem folosi terapeutic aceste descoperiri", spune Fernández-Capetillo.
În continuare, echipa îşi propune să găsească modalităţi de a reduce producţia de ribozomi, astfel încât deşeurile să scadă, păstrând în acelaşi timp un număr suficient pentru a garanta funcţionarea corectă a celulelor.
Cercetarea a fost publicată pe 22 martie în revista Molecular Cell.