Mielinizarea este esenţială pentru transmiterea rapidă a semnalelor electrice în creier, facilitând totul, de la mişcare la gândire. Distrugerea sau pierderea tecii de mielină care înconjoară axonii neuronilor, aşa cum se observă în afecţiuni precum scleroza multiplă şi alte boli neurodegenerative, duce la deficienţe cognitive şi fizice semnificative.
Un nou studiu realizat de oamenii de ştiinţă de la Institutul de neuroştiinţe Wu Tsai din cadrul Universităţii Stanford a identificat un factor cheie al mielinizării, adică al formării învelişurilor protectoare de grăsime din jurul fibrelor nervoase.
Noile descoperiri îi fac pe cercetători să fie entuziasmaţi de potenţialul unor noi căi de tratament pentru a reface aceste teci izolatoare la pacienţii cu afecţiuni demielinizante.
Cercetarea a fost publicată recent în revista în Proceedings of the National Academy of Sciences - PNAS.
Gena structurală SRF este esenţială pentru formarea mielinei
Studiul se concentrează asupra SRF (prescurtare de la „serum response factor" / factorul de răspuns seric), un factor de transcripţie cunoscut anterior pentru rolurile sale în diverse procese celulare, dar care nu a fost pe deplin înţeles în contextul mielinizării.
Prin intermediul unor tehnici sofisticate de biologie genetică şi moleculară, inclusiv analize ChIP-seq şi RNA-seq, echipa de cercetare a identificat SRF ca fiind un reglator esenţial al genelor implicate în structura celulară a oligodendrocitelor - celulele gliale responsabile de mielinizarea fibrelor nervoase din creier şi măduva spinării.
Pentru a crea mielină, oligodendrocitele învelesc fibrele nervoase cu sute de straturi de membrană celulară grasă proprie, extinzându-şi în acest proces de 25 până la 50 de mii de ori suprafaţa lor iniţială.
Această capacitate unică depinde de o reorganizare totală a schelei structurale a celulelor, în special a filamentelor de actină, care sunt esenţiale pentru structura şi mişcarea celulelor.
„Maşinăria celulară necesară pentru a forma aceste procese complexe de mielinizare şi pentru a alimenta această celulă sofisticată este incredibilă", a declarat Tal Iram, care şi-a făcut doctoratul la Institutul de Neuroştiinţe Wu Tsai, într-un comunicat.
Pentru a înţelege rolul SRF în formarea mielinei, echipa a creat modele „knock-out" de rozătoare lipsite de SRF în oligodendrocitele din creierul lor.
La aceste animale lipsite de SRF, cercetătorii au observat o reducere dramatică a nivelurilor de filamente de actină în timpul primelor etape ale diferenţierii celulare. Această deficienţă a împiedicat capacitatea celulelor de a forma învelişul de mielină din jurul axonilor.
Cercetătorii au fost, de asemenea, surprinşi să descopere că pierderea SRF a declanşat o semnătură genetică asociată anterior cu îmbătrânirea şi bolile neurodegenerative, cum ar fi boala Alzheimer.
„Cea mai neaşteptată descoperire a fost că SRF pare să reprime o semnătură transcripţională legată de boală", notrează Iram.
Această observaţie face legătura între noile descoperiri şi descoperirea recentă făcută de cercetătorii de la Stanford, conform căreia nivelurile de SRF din oligodendrocite scad odată cu vârsta la şoareci - şi că infuzarea animalelor în vârstă cu lichid cefalorahidian de la şoareci mai tineri poate stimula activarea SRF şi asamblarea actinei la niveluri mai tinereşti.
„Credem că şoarecele fără gena activă SRF ar putea imita ceea ce se întâmplă în creierul îmbătrânit, unde vedem mai puţin SRF în oligodendrocite", a explicat cercetătoarea.
Cercetarea ar putea duce la noi tratamente
Această cercetare nu numai că avansează înţelegerea fundamentală a oamenilor de ştiinţă cu privire la modul în care se formează mielina în creierul în curs de dezvoltare şi îşi păstrează integritatea la vârsta adultă, dar sugerează, de asemenea, că ţintirea căii genei SRF ar putea fi o abordare promiţătoare pentru tratarea tulburărilor legate de mielină.
Prin stimularea activităţii SRF, speculează cercetătorii, oamenii de ştiinţă ar putea fi capabili să promoveze mielinizarea, să o protejeze împotriva degradării sau chiar să o restabilească în contextul îmbătrânirii şi al bolilor neurologice.
„Există încă multe lucruri pe care nu le înţelegem despre mecanismele de supresie şi care sunt rolurile funcţionale ale acestor gene asociate cu boala sau îmbătrânirea", a mai precizat Iram, care acum continuă cercetările pentru a afla răspunsul la aceste întrebări în propriul său laborator de la Institutul de Ştiinţe Weizmann din Tel Aviv, Israel.
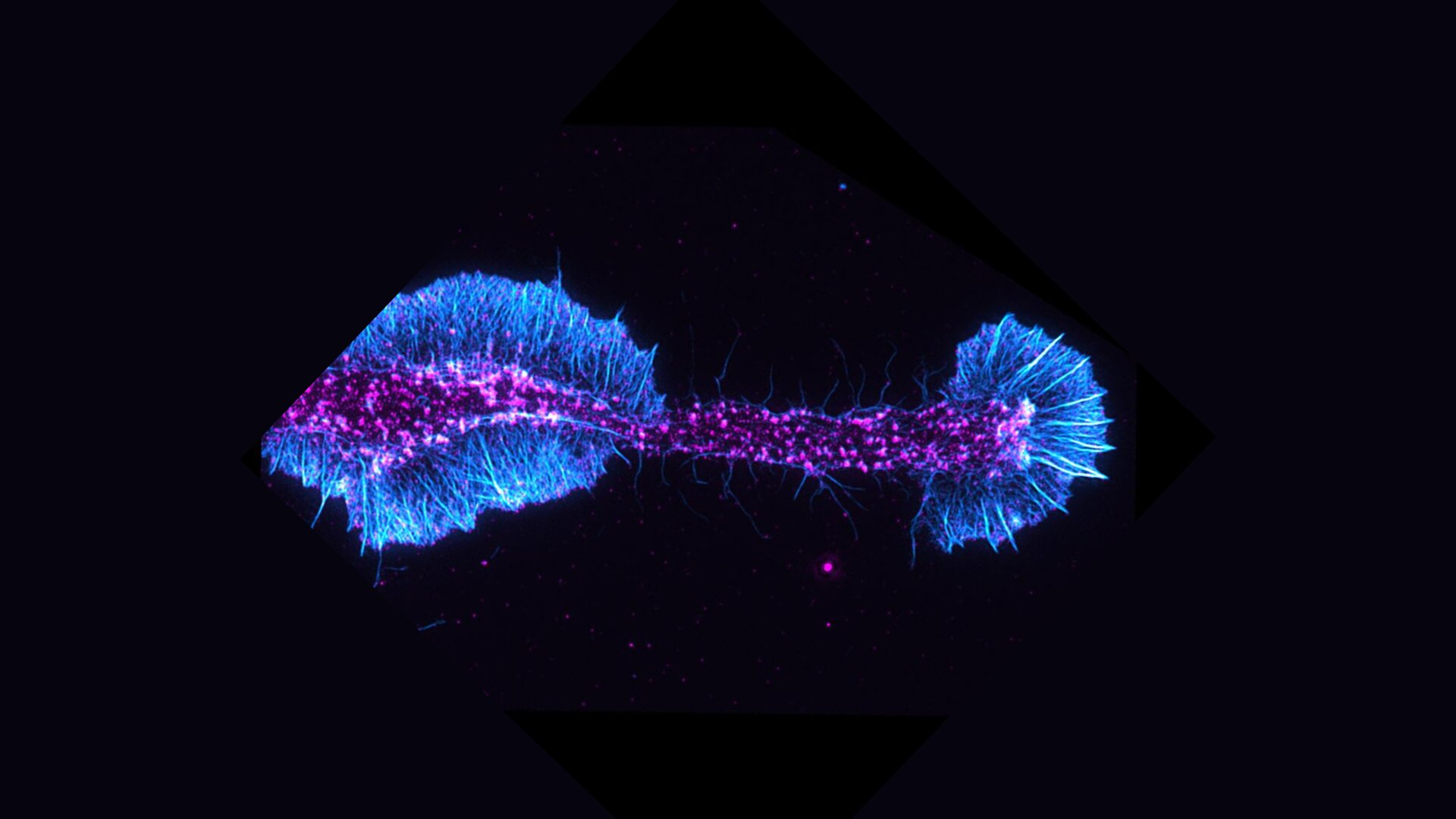
Foto: Filamente de actină (cyan) şi o proteină de reglare a actinei (magenta) într-un oligodendrocit în diferenţiere. Credit: Brad Zuchero şi Andrew Olson.