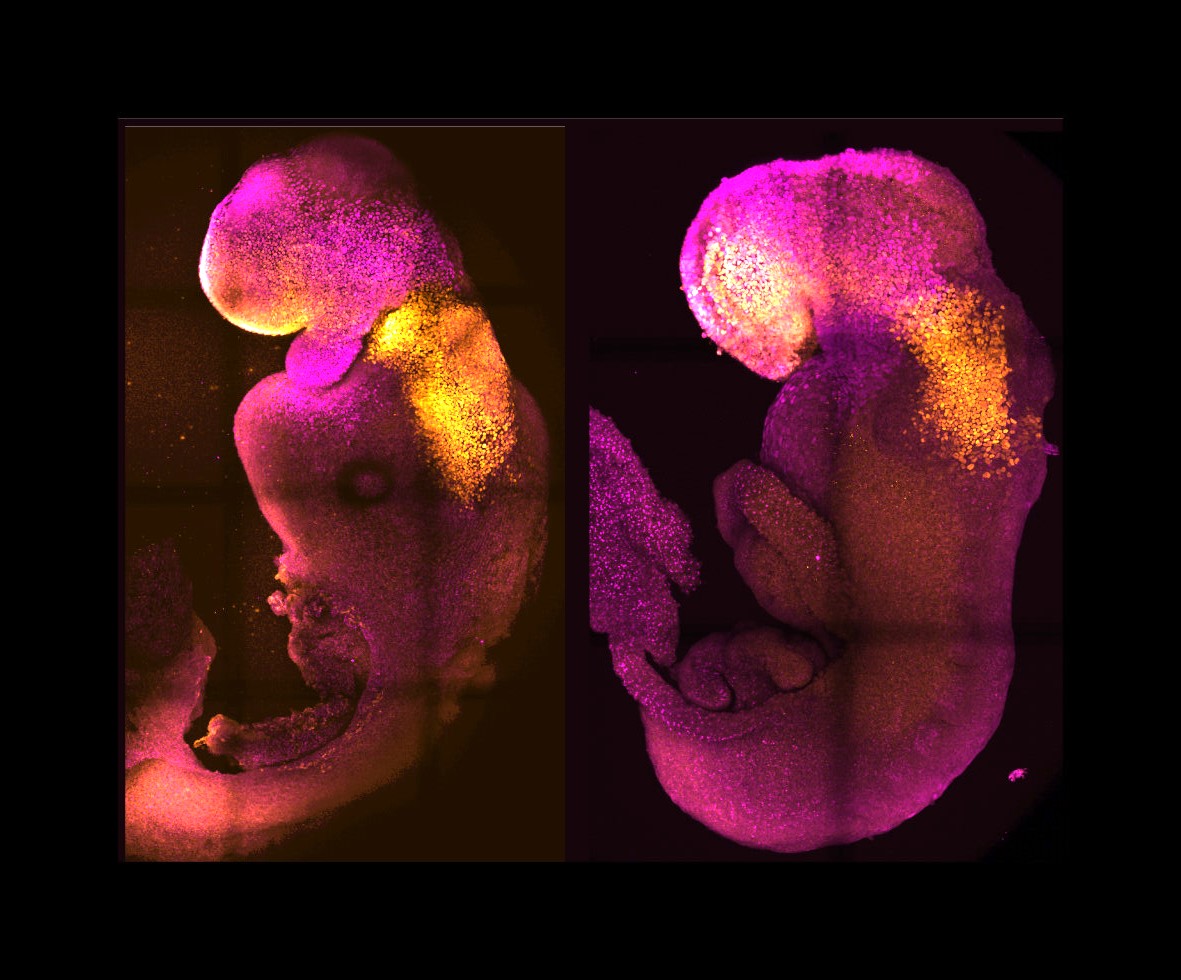
Cercetătorii de la universitatea din Cambridge au creat modele de embrioni din celule stem de şoarece, care formează un creier, o inimă care bate şi bazele tuturor celorlalte organe ale corpului, o nouă cale de a recrea primele etape ale vieţii.
O echipă de cercetători de la Cambridge, din Marea Britanie, a dezvoltat un model embrionar, fără ovule sau spermatozoizi, folosind celule stem, celulele primare ale corpului, care se pot dezvolta în aproape orice tip de celulă din organism.
Cercetătorii au imitat procesele naturale în laborator, ghidând cele trei tipuri de celule stem identificate în dezvoltarea timpurie a mamiferelor, până la punctul în care încep să interacţioneze. Prin inducerea expresiei unui anumit set de gene şi stabilirea unui mediu unic pentru interacţiunile celulare, cercetătorii au reuşit să determine celulele stem să „vorbească” între ele.
Celulele stem s-au autoorganizat în structuri care au progresat prin etapele succesive de dezvoltare până la nivelul la care au dezvoltat inimi care bat şi elemente de bază ale creierului, precum şi sacul vitelin unde se dezvoltă embrionul şi din care primeşte nutrienţi în primele săptămâni de viaţă.
Spre deosebire de alţi embrioni sintetici, modelele dezvoltate de Cambridge au ajuns în punctul în care întregul creier, inclusiv porţiunea sa anterioară, a început să se dezvolte.
Acesta este cel mai avansat nivel de dezvoltare embrionară care a fost atins până acum în cercetare, într-un model derivat din celule stem.
Echipa spune că rezultatele, care reprezintă mai mult de un deceniu de cercetări ce au condus progresiv la structuri asemănătoare embrionilor, şi care au fost publicate joi, în revista Nature, i-ar putea ajuta pe oamenii de ştiinţă să înţeleagă de ce unii embrioni eşuează, în timp ce alţii continuă să se dezvolte într-o sarcină sănătoasă.
În plus, rezultatele ar putea fi folosite pentru a ghida repararea şi dezvoltarea organelor umane sintetice pentru transplant.
„Modelul nostru de embrion de şoarece nu numai că dezvoltă un creier, ci şi o inimă care bate, şi toate componentele care formează corpul”, a spus a spus profesorul Magdalena Zernicka-Goetz, care a condus grupul de cercetare, şi care este profesor în dezvoltarea mamiferelor şi biologia celulelor stem la departamentul de fiziologie, dezvoltare şi neuroştiinţe de la Cambridge.
"Este de necrezut că am ajuns atât de departe. Acesta a fost visul comunităţii noastre de ani de zile şi obiectivul principal al muncii noastre timp de un deceniu şi, în sfârşit, am reuşit”.
Pentru ca un embrion uman să se dezvolte cu succes, trebuie să existe un „dialog” între ţesuturile care vor deveni embrion şi ţesuturile care vor conecta embrionul de mamă.
În prima săptămână după fertilizare, se dezvoltă trei tipuri de celule stem: una va deveni în cele din urmă ţesuturile corpului, iar celelalte două vor susţine dezvoltarea embrionului.
Unul dintre aceste tipuri de celule stem extraembrionare va deveni placenta, care leagă fătul de mamă şi furnizează oxigen şi substanţe nutritive; iar al doilea este sacul vitelin, unde creşte embrionul şi de unde îşi ia nutrienţii la începutul dezvoltării.
Multe sarcini eşuează în momentul în care cele trei tipuri de celule stem încep să-şi trimită semnale mecanice şi chimice unele către altele, care îi spun embrionului cum să se dezvolte corect.
„Atât de multe sarcini eşuează în această perioadă, înainte ca majoritatea femeilor să realizeze că sunt însărcinate”, a spus Zernicka-Goetz, care este şi profesor de biologie şi inginerie biologică la Caltech.
„Această perioadă este fundamentul pentru tot ce urmează în sarcină. Dacă merge prost, sarcina va eşua”, a spus omul de ştiinţă.
În ultimul deceniu, grupul prof. Zernicka-Goetz din Cambridge a studiat aceste etape incipiente ale sarcinii, pentru a înţelege de ce unele sarcini eşuează şi altele reuşesc.
„Modelul embrionului dezvoltat din celule stem este important pentru că ne oferă accesibilitate la structura în curs de dezvoltare, într-un stadiu care ne este în mod normal ascuns datorită implantării embrionului mic în uterul mamei”, a spus profesorul Zernicka-Goetz.
„Această accesibilitate ne permite să manipulăm genele pentru a înţelege rolurile lor în dezvoltare, într-un sistem experimental model”, a precizat cercetătoarea.
Pentru a ghida dezvoltarea embrionului sintetic, cercetătorii au reunit celule stem cultivate reprezentând fiecare dintre cele trei tipuri de ţesut, în proporţiile şi mediul potrivit, pentru a le promova creşterea şi comunicarea între ele, în cele din urmă acestea auto-asamblandu-se într-un embrion.
Cercetătorii au descoperit că celulele extraembrionare semnalizează celulelor embrionare prin semnale chimice dar şi mecanic, prin atingere, ghidând dezvoltarea embrionului.
„Această perioadă a vieţii umane este atât de misterioasă, încât pentru a putea vedea cum se întâmplă acest lucru, într-un vas, pentru a avea acces la aceste celule stem individuale, pentru a înţelege de ce atât de multe sarcini eşuează şi cum am putea preveni acest lucru, este destul de special”, a spus Zernicka-Goetz. „Ne-am uitat la dialogul care trebuie să aibă loc între diferitele tipuri de celule stem în acel moment, şi am arătat cum se întâmplă şi cum poate merge prost”, a mai comentat omul de ştiinţă.
Un progres major în studiu îl reprezintă capacitatea de a genera întregul creier, în special partea anterioară a creierului, care a fost un obiectiv major în dezvoltarea embrionilor sintetici. Acest lucru funcţionează în setarea Zernicka-Goetz, deoarece această parte a creierului necesită semnale de la unul dintre ţesuturile extraembrionare pentru a se putea dezvolta. Echipa s-a gândit că acest lucru ar putea fi posibil, încă din studiile lor din 2018 şi 2021, care au folosit aceleaşi celule componente şi au dezvoltat embrionii într-un stadiu mai puţin avansat faţă de reuşita din recentul studiu.
Acum, oamenii de ştiinţă pot spune definitiv că modelul lor este primul care arată semne de dezvoltare a creierului anterior şi, de fapt, a întregului creier.
„Acest lucru deschide noi posibilităţi de a studia mecanismele neurodezvoltării într-un model experimental”, a spus Zernicka-Goetz.
„De fapt, demonstrăm dovada acestui principiu în lucrare prin eliminarea unei gene despre care se ştie deja că este esenţială pentru formarea tubului neural, precursor al sistemului nervos şi pentru dezvoltarea creierului şi a ochilor. În absenţa acestei gene, embrionii sintetici prezintăaceleaşi exact defecte cunoscute în dezvoltarea creierului ca la un animal care poartă această mutaţie. Asta înseamnă că putem începe să aplicăm acest tip de abordare la numeroasele gene cu funcţie necunoscută în dezvoltarea creierului", a explicat omul de ştiinţă.
În timp ce recentele cercetări au fost efectuate pe modele de şoarece, cercetătorii dezvoltă şi modele umane similare, cu potenţialul de a fi direcţionate către generarea de tipuri specifice de organe, pentru a înţelege mecanismele din spatele proceselor cruciale care altfel ar fi imposibil de studiat în embrioni reali.
În prezent, legea britanică permite studierea embrionilor umani în laborator doar până în a 14-a zi de dezvoltare.
Dacă aplicaţiile dezvoltate de echipa Zernicka-Goetz vor avea succes, în viitor, şi cu celulele stem umane, ar putea fi folosite şi pentru a ghida dezvoltarea organelor sintetice pentru pacienţii care aşteaptă transplanturi.
„Există atât de mulţi oameni în întreaga lume care aşteaptă ani de zile pentru transplanturi de organe”, a comentat Zernicka-Goetz.
„Ceea ce face ca munca noastră să fie atât de interesantă este faptul că am putea folosi cunoştinţele rezultate pentru a creşte organe umane sintetice corespunzătoare pentru a salva acele vieţi, pe care, în prezent, le pierdem. De asemenea, ar trebui să fie posibil să intervenim şi să vindecăm organele adulte, folosind cunoştinţele pe care le avem despre cum se formează.„Acesta este un pas incredibil înainte şi a fost nevoie de 10 ani de muncă grea din partea multor membri ai echipei mele, nu m-am gândit niciodată că vom ajunge în acest loc. Niciodată nu crezi că visele tale vor deveni realitate, dar iată că acest lucru s-a întâmplat”, a mai spus omul de ştiinţă.