Folosind un model animal de boală Alzheimer nou, un recent studiu evidenţiază o potenţială descoperire în strategiile de tratament. Spre deosebire de terapiile actuale, care vizează în principal o singură proteină toxică legată de boală, această cercetare explorează o abordare mai cuprinzătoare.
O echipă de cercetare de la Institut de Neuroştiinţe din cadrul Universităţii din Barcelona (INc-UAB) a identificat modul în care cele două caracteristici principale ale bolii Alzheimer - proteina tau şi beta-amiloidul - afectează circuitele cerebrale în moduri distincte, dar complementare, în special cele implicate în memorie şi emoţii.
Studiul, realizat în colaborare cu Centrul pentru Reţeaua de cercetare biomedicală privind bolile neurodegenerative (CIBERNED) şi Universitatea Pablo de Olavide (UPO), oferă noi perspective asupra mecanismelor care stau la baza bolii.
Publicată recent în revista Molecular Psychiatry, cercetarea arată că acumularea de tau în hipocampus contribuie în primul rând la deficitele de memorie, în timp ce acumularea de beta-amiloid în amigdală duce la tulburări emoţionale precum anxietatea şi frica - ambele fiind simptome timpurii ale bolii Alzheimer. În plus, prezenţa ambelor patologii împreună exacerbează inflamaţia şi disfuncţia creierului, amplificând impactul lor general asupra sănătăţii cognitive şi emoţionale.
Timp de decenii, cercetarea privind boala Alzheimer a fost modelată de două teorii: una care sugerează că boala îşi are originea în acumularea de tau în interiorul neuronilor, iar alta care indică acumularea de beta-amiloid ca principal factor declanşator. Aceste perspective au dictat în mare măsură abordările terapeutice actuale, tratamentele vizând prevenirea acumulării de tau sau beta-amiloid în speranţa încetinirii progresiei bolii.
Cu toate acestea, echipa de oameni de ştiinţă condusă de cercetătorii Carles Saura şi Arnaldo Parra-Damas, de la Departamentul de biochimie şi biologie moleculară al UAB şi de la INc-UAB, susţine că o strategie terapeutică cu dublă ţintă poate fi necesară pentru a combate eficient această boală.
Un nou model transgenic de şoarece
Această descoperire a fost posibilă prin dezvoltarea unui nou model de şoarece transgenic care reproduce atât patologiile tau, cât şi cele beta-amiloide.
„Deşi ambele proteine se acumulează în creierul pacienţilor cu Alzheimer, majoritatea modelelor animale utilizate pentru studierea bolii se concentrează de obicei doar pe unul dintre aceşti factori”, explică cercetătoarea Maria Dolores Capilla, autorul principal al studiului, într-un comunicat.
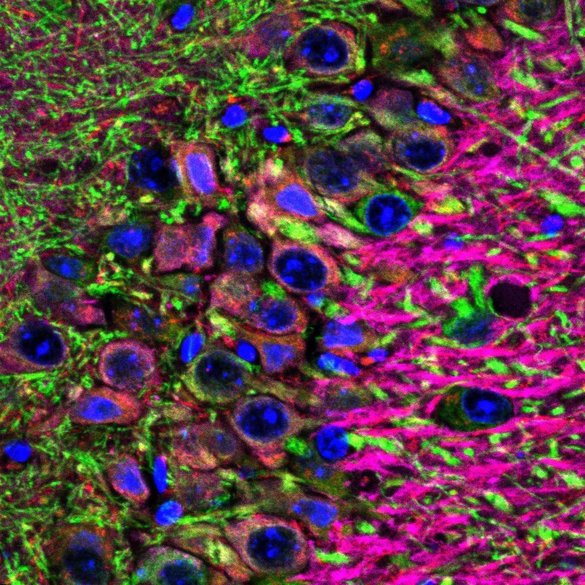
Imaginea neuronilor din hipocampus care reglează memoria sunt afectaţi de patologia bolii Alzheimer în modelul de şoarece generat în cadrul studiului. Credit: UAB, 6 februarie 2025
„În cercetarea noastră, am generat un model de şoarece transgenic care prezintă atât acumulare de tau, cât şi de beta-amiloid, permiţându-ne să analizăm efectele lor individuale şi combinate”, adaugă cercetătorul INc-UAB.
Aceste descoperiri ar putea remodela strategiile actuale de tratament, care adesea vizează doar una dintre aceste proteine toxice.
„Terapiile existente nu au obţinut beneficii clinice clare. Studiul nostru sugerează că o abordare terapeutică care abordează mai multe mecanisme ale bolii - cum ar fi tau fosforilat şi beta-amiloid - ar putea fi mai eficientă”, conchide Carles Saura.
Deşi sunt necesare cercetări suplimentare pentru a confirma aplicabilitatea la om, acest studiu reprezintă un pas semnificativ către noi căi de investigare pentru tratamentul Alzheimer, conchide echipa de cercetare.

Foto: Echipa de cercetare de la INc-UAB care a realizat studiul. De la stânga la dreapta: Ángel Deprada, Arnaldo Parra-Damas, Paula Sotillo, Carles Saura y Maria Dolores Capilla-López. Credit: UAB, 6 februrie 2025.





