Căutând noi abordări de tratament pentru cancerul pediatric, o echipă de oameni de ştiinţă de la spitalul pentru copii, St. Jude, din Statele Unite, a vizat un proces considerat până acum greu de ţintit şi netratabil, reuşind să identifice o nouă strategie de tratament pentru o formă agresivă de rabdomiosarcom.
Strategia implică vizarea clasei de proteine KDM4, pentru tratamentul rabdomiosarcomului alveolar condus de fuziunea genelor PAX3-FOXO1.
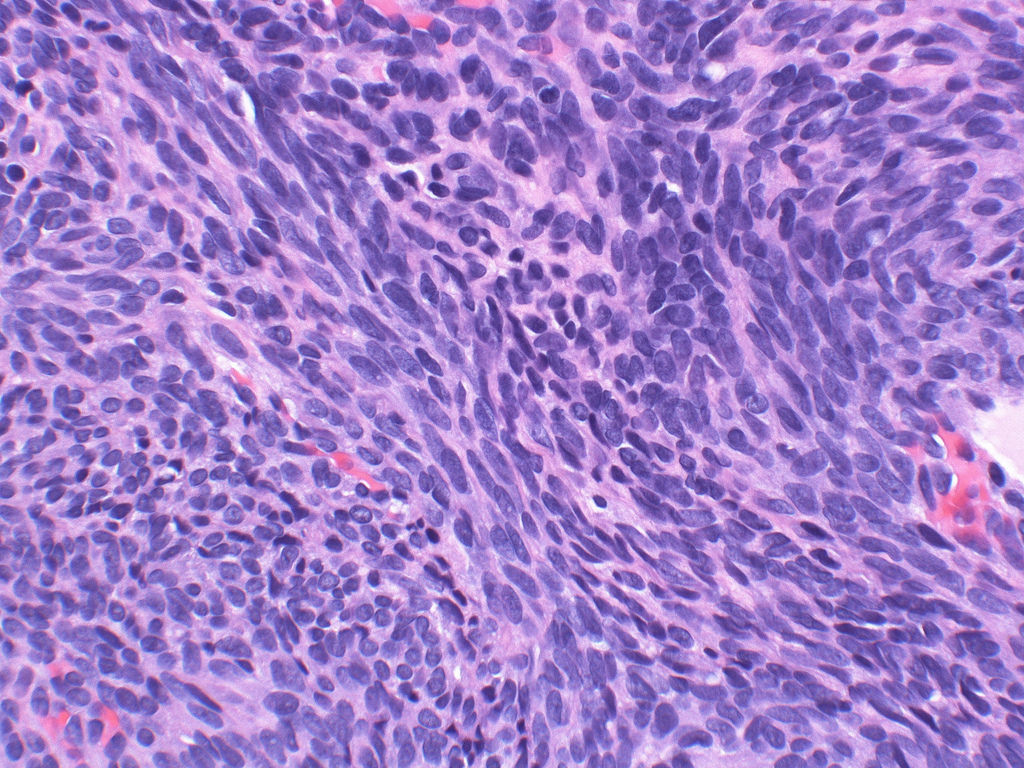
Rabdomiosarcomul este un tip de tumoră malignă (canceroasă), care apare în ţesuturile moi, inclusiv în muşchi.
Sarcomurile ţesuturilor moi reprezintă 7-8% dintre toate cancerele pediatrice.
Există două tipuri de rabdomiosarcoame: embrionare şi alveolare. Tipul alveolar apare la copiii de toate vârstele şi afectează adesea muşchii mari ai braţelor, picioarelor şi trunchiului.
Când o bucată dintr-o genă se leagă anormal de o alta, are loc o fuziune genetică şi ia naştere o genă hibridă. Împreună, aceste fragmente genetice (gena hibridă) codifică o oncoproteină de fuziune, care joacă un rol în dezvoltarea cancerului.
Rabdomiosarcomul alveolar conţine fuziunea PAX3-FOXO1 şi este mai agresiv, având o rată mai mare de metastază şi un prognostic mai sărac decât cancerele fără această fuziune.
„Rabdomiosarcomul condus de această fuziune este o boală periculoasă, care este foarte dificil de vindecat. Are câteva mutaţii genetice care îl conduc şi opţiuni limitate de tratament pentru tipurile pozitive cu această fuziune. Analizând o clasă de proteine care elimină semnele de metilare din histone, am reuşit să identificăm o ţintă promiţătoare care a trecut neobservată până acum. În combinaţie cu standardul de îngrijire (chimioterapia), am văzut un răspuns complet în modelele noastre, care au fost de cele mai multe ori foarte rezistente când au primit doar chimioterapie”, a declarat autorul corespondent al studiului, dr. Jun Yang, de la departamentul de chirurgie al spitalului St Jude.
Procesul genetic de transcriere
Factorii de transcriere sunt proteine implicate în procesul de „transcriere” sau de conversie a informaţiilor din ADN în ARN. Transcrierea este un proces biologic esenţial, deoarece copia ARN a secvenţei ADN a unei gene este utilizată pentru a produce proteine. Transcrierea este în mod normal un proces strict controlat, dar în celulele canceroase, acest process poate fi dereglat. Această dereglare face ca celulele canceroase să devină dependente de proteine anormale sau de factori implicaţi în proces.
Circuitul de bază pentru reglarea transcripţiei (CRC) se referă la un set de factori de transcriere care stabilesc şi menţin identitatea celulei (ce fel de celulă este şi cum funcţionează). Fuziunea PAX3-FOXO1 este o anomalie genetică care afectează factorii de transcriere care joacă un rol esenţial în construirea unei reţele CRC pentru rabdomiosarcom.
„Aceşti factori de transcriere sunt foarte greu de ţintit pentru că nu au un buzunar de legare (regiuni de pe proteine care le permit să se lege de molecule care au o anumită specificitate), deci este greu să dezvolţi orice medicament care se poate lega de ei. Celulele canceroase se bazează pe aceşti factori de transcriere şi pe reţeaua lor de reglare CRC. Prin vizarea proteinelor partenere ale CRC, în acest caz KDM4B, am descoperit că putem distruge această reţea, şi să tratăm în mod eficient cancerul”, a declarat coautoarea studiului dr. Shivendra Singh, de la departamentul de chirurgie al spitalului St. Jude.
Pentru a studia fuziunea PAX3-FOXO1 şi a identifica rolurile diferitelor părţi ale reţelei, cercetătorii au efectuat analize sofisticate, inclusiv secvenţiere ARN, metoda CUT&TAG (tehnică prin care cercetătorii pot studia interacţiunile dintre proteine şi ADN pentru a identifica zonele de legare ale proteinelor de interes), şi secvenţierea ATAC (o metodă de secvenţiere a genomului de nouă generaţie, care se bazează pe transpozaza Tn5).
Oamenii de ştiinţă au reuşit să identifice astfel KDM4B, şi au descoperit că reprezintă un nod important în reţeaua CRC a rabdomiosarcomului alveolar condus de oncogenele de fuziune.
„Acest studiu a fost o călătorie foarte lungă, pentru a înţelege mecanismele din spatele motivului pentru care inhibarea KDM4 pare atât de reuşită în acest subtip de rabdomiosarcom. Am reuşit să urmărim conexiunile importante dintre KDM4 şi circuitele de bază care controlează acest cancer”, a declarat dr. Hongjian Jin, de la central pentru bioinformatică aplicată, de la St. Jude, unul dintre autorii principali ai studiului.
Strategie pentru un nou tratament
Factorii de transcriere sunt dificil de ţintit cu tratamente, dar interacţiunea lor cu alte proteine oferă cercetătorilor oportunitatea de a viza aceste proteine partenere şi de a le perturba activitatea.
Folosind metode genetice şi un compus care inhibă KDM4B, cercetătorii au reuşit să întârzie substanţial creşterea tumorii în laborator. Inhibarea KDM4B în combinaţie cu regimuri de chimioterapie, utilizate în prezent ca tratament, a cauzat micşorarea tumorilor în modelele preclinice de xenogrefe cu acest tip de cancer.
„Am căutat reglatori epigenetici în amonte, care să poată regla aceşti factori de transcriere şi am identificat în mod specific KDM4 ca fiind unul dintre aceşti reglatori, ceea ce este o noutate în sine. De asemenea, am testat o terapie ţintită în acest model de cancer, în combinaţie cu chimioterapia, care a demonstrat un efect anticancer foarte eficient. În această boală, nu s-a mai încercat pînă acum inhibarea KDM4, ceea ce este iarăşi, extraordinart”, a declarat Ahmed Abu-Zaid, de la departamentul de chirurgie St. Jude, unul dintre coautorii studiului.
Un inhibitor ţintit al KDM4B este testat clinic în prezent pentru cancerul de colon adult. Urmează cercetări suplimentare înainte ca abordarea să poată fi transpusă într-un studiu clinic pentru copiii cu rabdomiosarcom.
Concluziile cercetării au fost publicate în Science Translational Medicine.