Un tratament care a folosit CRISPR s-a dovedit a fi sigur şi eficient în îmbunătăţirea vederii în rândul unui mic eşantion de pacienţi cu orbire ereditară în cadrul studiului clinic de fază I/II. Degenerările ereditare ale retinei reprezintă una dintre principalele cauze de orbire în întreaga lume.
Pentru copiii născuţi cu o formă rară de orbire infantilă numită amauroză congenitală Leber (LCA), adesea cauzată de o singură mutaţie genetică, un nou tratament inovator care utilizează tehnologia de editare genetică CRISPR prezintă rezultate promiţătoare în ceea ce priveşte restabilirea vederii.
LCA este o afecţiune genetică care afectează retina, ţesutul sensibil la lumină din spatele ochiului, responsabil pentru detectarea luminii şi a culorilor.
Copiii cu LCA se confruntă adesea cu o pierdere severă a vederii sau orbire completă de la o vârstă foarte fragedă. Una dintre cele mai frecvente cauze ale LCA este un defect în gena CEP290, care joacă un rol crucial în dezvoltarea şi funcţionarea celulelor sensibile la lumină ale retinei, numite fotoreceptori.
Până în prezent, nu au existat tratamente eficiente pentru LCA care rezultă din mutaţiile CEP290. Cu toate acestea, noul studiu condus de cercetătorii de la Massachusetts Eye and Ear şi Universitatea pentru ştiinţă şi sănătate din Oregon oferă o rază de speranţă.
Într-un studiu restrâns, care a inclus un total de 14 voluntari, cercetătorii au testat o terapie nouă numită EDIT-101 pe pacienţi cu LCA. S-a constatat că instrumentul de editare genetică a fost asociat cu o „îmbunătăţire semnificativă” a vederii pentru majoritatea pacienţilor la aproximativ trei luni după tratamentşi nu a fost direct legat de efecte secundare grave, potrivit rezultatelor studiului, publicate luni în revista New England Journal of Medicine, NEJM.
Terapia este în prezent experimentală, iar rezultatele trebuie să fie reproduse pe un grup mai mare de persoane.
O „dovadă a conceptului revoluţionară”
Studiul, început în 2020, reprezintă o premieră, fiind pentru prima dată când tehnologia de editare genetică CRISPR a fost folosit pe ochii unor persoane vii.
„Rezultatele acestui studiu oferă o dovadă de concept că editarea genetică CRISPR-Cas9 poate fi utilizată în siguranţă şi în mod eficient pentru a trata tulburările retiniene moştenite”, a declarat primul autor al studiului, dr. Eric Pierce, director al Institutului de genomică oculară din cadrul Mass Eye and Ear şi facultăţii de medicină a universităţii Harvard.
Studiul a fost finanţat de compania de biotehnologie Editas Medicine şi a fost realizat în Statele Unite de cercetători de la Mass Eye and Ear din cadrul sistemului de sănătate Mass General Brigham şi de la alte instituţii universitare din Statele Unite, inclusiv de la facultatea de medicină Perelman de la universităţile din Pennsylvania, Michigan, Miami şi Universitatea pentru ştiinţă şi sănătate din Oregon.
„Suntem foarte încrezători că tehnologiile de editare genetică CRISPR-Cas9 vor fi acum aplicate şi la alte forme genetice de orbire ereditară şi la alte boli genetice în general”, a mai precizat dr. Pierce. „Sperăm că studiul va contribui la deschiderea unei noi ere pentru utilizarea terapeutică a tehnologiilor CRISPR-Cas9”, a adăugat medicul.
Studiul, care a început în 2019, a înrolat 12 adulţi, cu vârste cuprinse între 17 şi 63 de ani, şi doi copii, cu vârste de 9 şi 14 ani, cu degenerescenţă retiniană ereditară cauzată de mutaţii în gena CEP290.
Gena respectivă furnizează instrucţiuni pentru fabricarea unei proteine implicate în multe tipuri de celule, inclusiv în celulele receptoare de lumină din ochi. Mutaţiile în CEP290 sunt cea mai frecventă cauză a degenerării severe a retinei cu debut precoce, care provoacă pierderea vederii la copii.
În prezent, nu există niciun tratament aprobat pentru degenerescenţa retiniană ereditară asociată cu CEP290. Aceşti pacienţi nu ar fi capabili să citească niciun rând de litere sau numere de pe diagrama folosită la examinăarălie din cabinetele medicilor oftalmologi, iar deficienţa vizuală se poate agrava în timp.
În cadrul studiului, cei 14 participanţi au fost supuşi unei proceduri chirurgicale prin care un medicament numit EDIT-101 care codifică componentele de editare genetică CRISPR a fost injectat sub retina unuia dintre ochi.
Deoarece studiul a fost efectuat în principal pentru a evalua siguranţa şi eficacitatea, a fost aplicat doar pe un singur ochi la fiecare pacient.
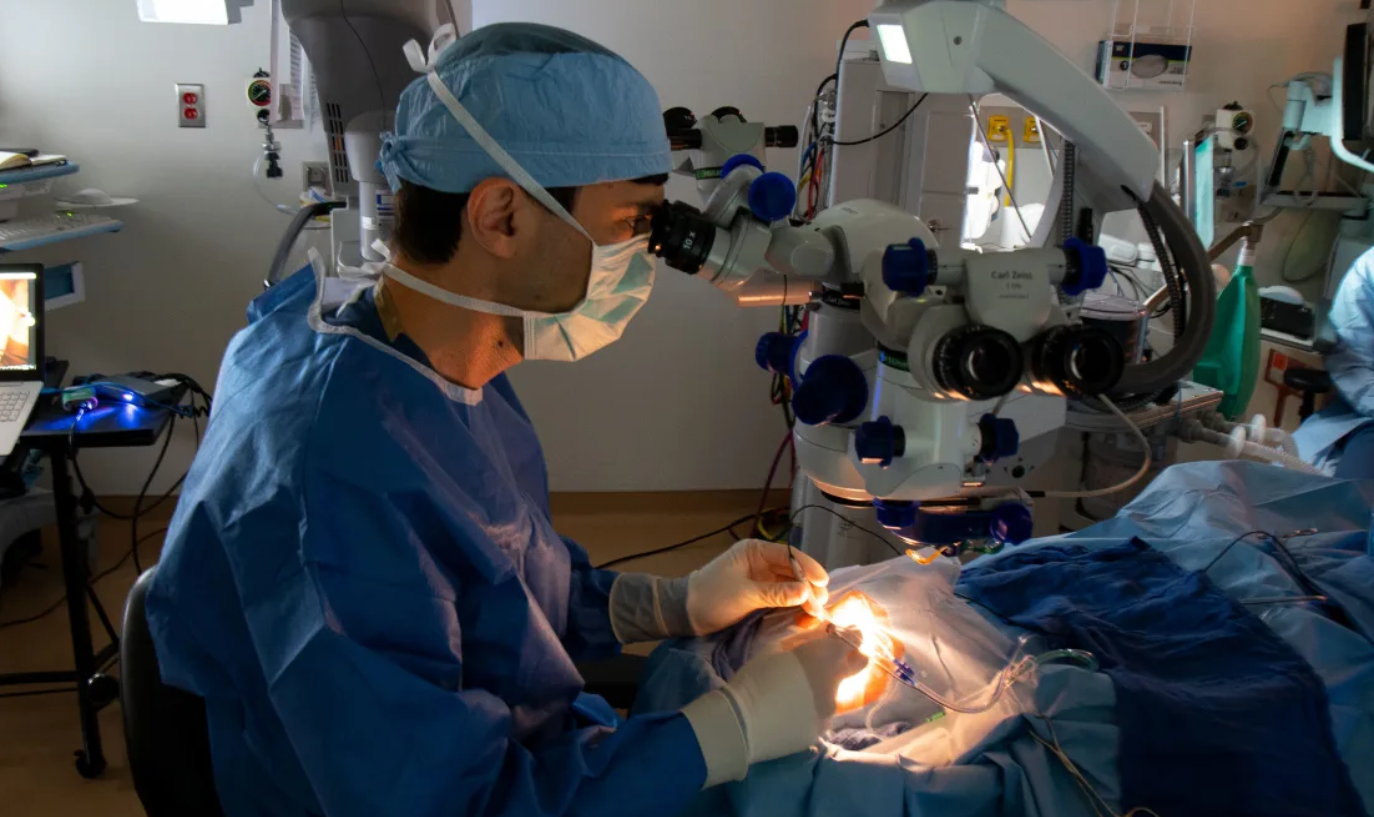 Dr. Jason Comander efectuează procedura chirurgicală pentru a administra medicamentul experimental bazat pe CRISPR unui participant la studiu în septembrie 2020.Credit: Mass Eye and Ear
Dr. Jason Comander efectuează procedura chirurgicală pentru a administra medicamentul experimental bazat pe CRISPR unui participant la studiu în septembrie 2020.Credit: Mass Eye and Ear
„Participanţii primesc o injecţie cu medicamentul de editare genetică, numit EDIT-101, sub retină”, explică dr. Pierce. „Acest medicament codifică maşinăria de editare genetică CRISPR-Cas9 şi, odată ce aceasta începe să funcţioneze în interiorul celulelor retinei acestor pacienţi, elimină mutaţia din CEP290 din genomul celulelor retinei lor, permiţând restabilirea funcţiei genei CEP290”.
Atunci când primii pacienţi din cadrul studiului au fost trataţi în 2020, a fost pentru prima dată în istoria medicală când un medicament bazat pe CRISPR, având ca rezultat editarea genetică, a fost introdus direct în corpul uman viu.
Dintre voluntarii adulţi, doi au primit o doză mică de medicament, cinci au primit o doză intermediară şi cinci au primit o doză mare.
Ambilor copii din cadrul studiului li s-a administrat doza intermediară. Procedura ambulatorie a durat aproximativ o oră şi jumătate.
Pacienţii au fost apoi monitorizaţi la fiecare trei luni timp de un an, iar apoi monitorizarea mai puţin frecventă a continuat timp de doi ani. În cadrul acestor vizite de monitorizare, pacienţii au fost supuşi, printre alte evaluări, la o serie de teste de vedere.
Cercetătorii au constatat că 11 pacienţi din studiu au avut un anumit tip de îmbunătăţire a vederii în urma terapiei CRISPR, iar aceste îmbunătăţiri au apărut la aproximativ trei luni după procedură şi au fost menţinute în timpul vizitelor ulterioare.
De asemenea, potrivit cercetătorilor, nu au apărut efecte secundare grave ca răspuns la tratament la niciuna dintre doze, iar evenimentele adverse care au apărut au fost uşoare sau moderate. De asemenea, nu au existat semne că editarea genetică CRISPR ar fi provocat daune cu efect de undă asupra genomului pacienţilor.
„Scopul principal al acestui studiu în premieră la om a fost acela de a testa siguranţa utilizării editării genetice CRISPR-Cas9 in vivo. Când am început studiile, subiecţii care au fost trataţi au fost primii pacienţi care au primit vreodată tratamente de editare genetică CRISPR-Cas9 in vivo", a declarat dr. Pierce. „Nu au existat evenimente adverse grave legate de tratament sau de intervenţia chirurgicală necesară pentru administrarea tratamentului şi nu au existat toxicităţi care să limiteze doza”
În urma intervenţiei chirurgicale, un pacient a prezentat unele sângerări la nivelul ochiului, care i-au afectat vederea, dar acest lucru s-a rezolvat între timp, potrivit cercetătorilor.
„Odată ce hemoragia respectivă s-a eliminat, vederea subiectului a revenit la nivelul de bază”, a menţionat dr. Pierce.
Un alt pacient a prezentat tulburări de vedere asociate cu mici umflături observate sub retină la şase luni după procedură. Aceste tipuri de umflături au fost observate în alte studii care au implicat terapii genice subretiniene, au remarcat cercetătorii, iar cauza lor nu este deocamdată clară.
„Se crede că este vorba de inflamaţie”, a menţionat dr. Pierce.
Pacienţii au fost tratat cu un curs de medicamente cu steroizi, potrivit studiului, iar recuperarea lor este în curs de desfăşurare.
„Pe măsură ce umflăturile s-au rezolvat, s-a îmbunătăţit şi vederea acestora”, a precizat dr. Pierce. „Cred că acest medicament a fost cât se poate de sigur din punct de vedere al designului”.
Totuşi, vederea completă nu a fost restabilită în rândul pacienţilor.
Cei mai mulţi dintre participanţii la studiu nu puteau citi nicio linie a unei diagrame oculare înainte de studiu şi doar patru dintre ei au înregistrat unele îmbunătăţiri ale acestei abilităţi.
Dar unii pacienţi au raportat, după ce au primit tratamentul, că au putut să distingă lumina telefonului mobil, să diferenţieze diverse alimente din farfurie, să identifice pictograma Apple care se roteşte pe ecranul unui computer sau chiar să observe apusul soarelui.
„Am început să văd ceea ce sunt descrise ca explozii de culoare”, a declarat Michael Kalberer, în vârstă de 46 de ani, care a primit tratamentul CRISPR la ochiul drept şi a observat pentru prima dată îmbunătăţiri ale vederii sale după aproximativ două până la şase luni. El a început studiul în 2020.
„A fost un moment destul de cool să văd cum luminile stroboscopice de pe ringul de dans de la nunta vărului meu îşi schimbă culoarea”, a spus Kalberer, care a adăugat că, dacă nu ar fi primit tratamentul, tot ce ar fi văzut pe ringul de dans ar fi fost umbre şi lumini pâlpâitoare şi nu ar fi putut identifica culorile.
 Michael Kalberer, participant la studiu, la o întâlnire de monitorizare după ce a primit terapia experimentală bazată pe CRISPR. Credit: Mass Eye and Ear
Michael Kalberer, participant la studiu, la o întâlnire de monitorizare după ce a primit terapia experimentală bazată pe CRISPR. Credit: Mass Eye and Ear
Specialiştii descriu tratamentul CRISPR ca fiind „revoluţionar”, dar avertizează că nu este un remediu definitiv pentru orbire.
„Nu este un panaceu”, a spus Kalberer, care încă nu poate vedea text standard sau fotografii pe un ecran. „Încă am boala. Nu a dispărut. Nu sunt vindecat. Dar cu siguranţă a încetinit progresia ei” a declarat pacientul.
Dr. Pierce speră ca această abordare a utilizării CRISPR ca terapie pentru orbirea ereditară să poată fi studiată din nou pe un grup mai mare şi mai divers de pacienţi. Toţi participanţii la studiul de fază I/II au fost non-hispanici şi albi.
În 2022, Editas Medicine a anunţat că a pus în pauză continuarea studiului de editare genetică CRISPR ca abordare terapeutică pentru orbirea ereditară asociată cu CEP290 şi, în loc să efectueze alte studii, a continuat să urmărească pacienţii care au fost trataţi până în prezent.
Cele mai recente rezultate ale studiului de fază I/II susţin continuarea cercetărilor cu un studiu de fază III şi apoi înregistrarea terapiei în vederea unei posibile aprobări de către autoritatea americană de reglementare din domeniul sănătăţii, FDA, a dmai precizat dr. Pierce.
„Lucrăm cu Editas pentru a identifica un partener comercial suplimentar pentru studiile de fază 3. De fapt, sperăm ca aceste rezultate publicate să stimuleze interesul comunităţilor de biotehnologie şi farmaceutice în acest sens", a declarat dr. Pierce, pentru CNN.
Mai multe cercetări în timp ar putea face lumină asupra efectelor pe termen lung ale instrumentelor de editare genetică CRISPR-Cas9.
„Cred că adevăratul risc de care suntem cu toţii îngrijoraţi în legătură cu editarea genetică prin tehnologia CRISPR-Cas9 este dacă nu cumva maşinăria de editare genetică pe care am introdus-o în celulele retinei acestor pacienţi să facă altceva, în altă parte în genom, pe lângă activităţile terapeutice pentru care a fost concepută”, a precizat dr. Pierce.
„Ar putea fi efectuată o astfel de modificare în genom peste 10 ani, care ar putea avea un efect advers în timp? Cred că răspunsul la această întrebare este da, ar putea. Dar avem speranţa că acest risc este foarte scăzut", a precizat dr. Pierce. „Pentru asta avem nevoie de o monitorizare suplimentară”, a accentuat el.
Dar calitatea vieţii contează.
Rezultatele studiului de fază I/II şi modul în care pacienţii au experimentat unele îmbunătăţiri ale vederii reprezintă un memento valoros despre cât de importantă poate fi calitatea vieţii pentru pacienţi, a precizat Art Caplan, profesor de bioetică şi şeful fondator al deiviziei de etică medicală la departamentul de sănătate a Populaţiei de la facultatea de medicină NYU Grossman.
„De obicei, atunci când facem terapii genetice sau alte intervenţii inovatoare, le asociem cu salvarea de vieţi. Acest experiment este un memento uriaş care ne aminteşte că şi calitatea vieţii contează", a precizat Caplan. „Nimeni nu moare. Nimeni nu este salvat. Dar restabilirea vederii este o realizare importantăcare ne reaminteşte că şi calitatea vieţii trebuie să fie luată în considerare atunci când decidem ce terapii să fie acoperite de asigurarea medicală, şi ceea ce încercăm să studiem”, a mai precizat acesta.
El a fost de acord cu cercetătorii că ar fi utile mai multe date privind siguranţa în timp.
„Pentru aceste tipuri de intervenţii genetice, trebuie să facem o monitorizare pe perioade lungi de timp - ani - pentru a ne asigura că alte gene nu au fost afectate”, a subliniat cercetătorul.
El a mai precizat că aceste noi rezultate ale studiului de fază I/II oferă o „piatră de temelie” pentru cercetările viitoare care-şi propun dezvoltarea de terapii genice pentru tratarea tulburărilor oculare,





