O nouă cale care minimizează leziunile hepatice în timpul transplantului ar putea duce la rezultate mai bune pentru pacienţi, potrivit unui studiu al specialiştilor americani, publicat miercuri.
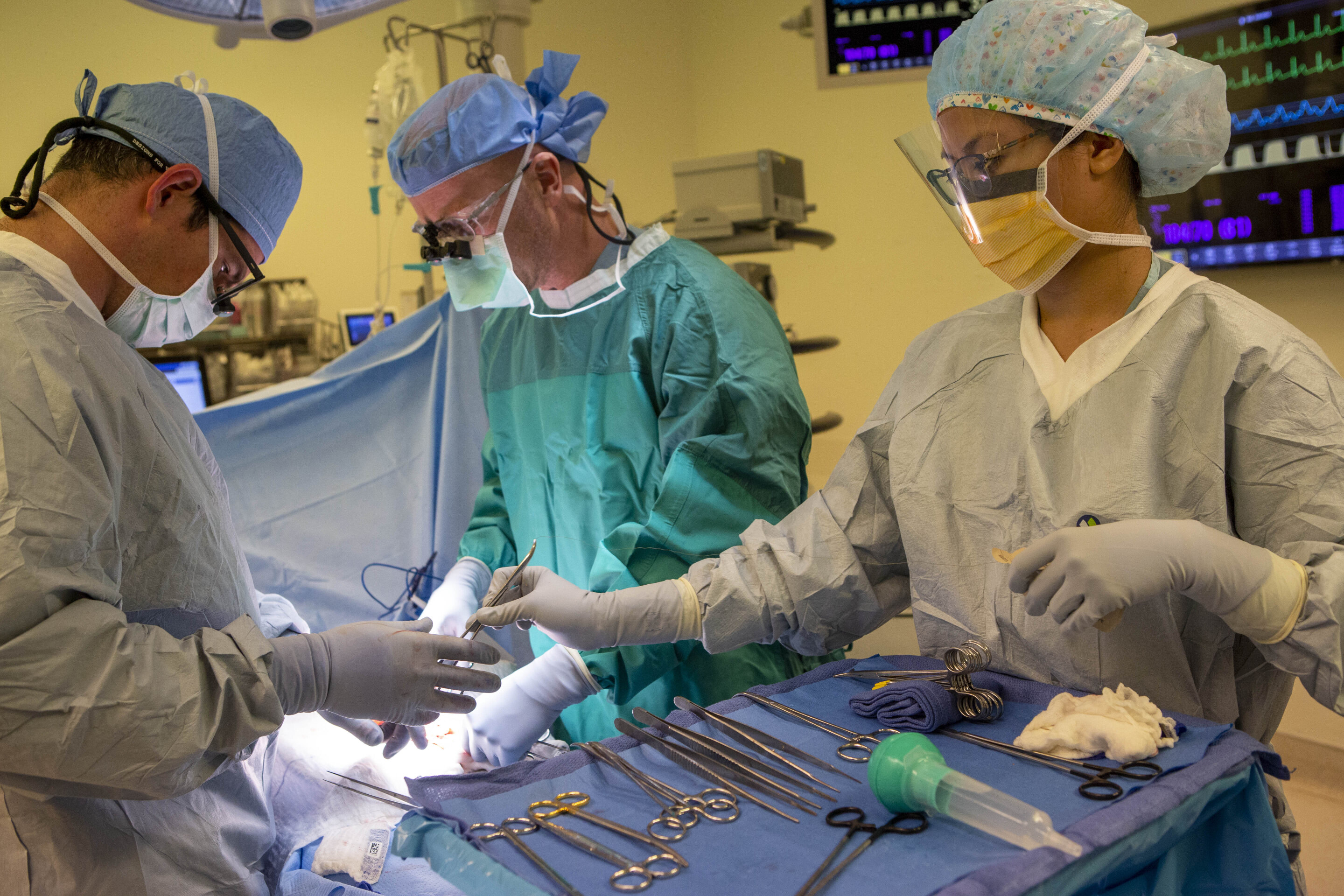
O cercetare condusă de UCLA descrie rolul pe care îl joacă o proteină numită CEACAM1 în protejarea ficatului de leziuni în timpul procesului de transplant, ceea ce ar putea îmbunătăţi rezultatele transplantului (foto credit: UCLA Health)
Într-un studiu, publicat online, în Science Translational Medicine, o echipă de cercetători a identificat factorii moleculari care stau la baza acestei protecţii şi a arătat cum, prin utilizarea instrumentelor moleculare şi a splicingului alternativ al genelor, CEACAM1 poate deveni mai protectoare, reducând astfel leziunile organului şi îmbunătăţind în cele din urmă rezultatele post-transplant.
Înainte de transplant, un organ solid, cum ar fi ficatul, nu are flux sanguin şi, prin urmare, nu are oxigen.
Aprovizionarea cu sânge este readusă la organ în timpul transplantului, dar acest proces poate provoca inflamaţii şi leziuni tisulare numite leziuni de reperfuzie ischemică, cunoscute şi sub numele de leziuni de reoxigenare.
În mod specific, cercetătorii au descoperit că factorul 1 indus de hipoxie (HIF-1α), care reglează consumul de oxigen, a jucat un rol central în orchestrarea activării versiunii de CEACAM1, numită CEACAM1-S, care limitează leziunile celulare şi îmbunătăţeşte funcţia hepatică la şoareci.
De asemenea, ei au descoperit că această relaţie dintre CEACAM1-S şi HIF-1 în ficatul donatorilor la om prezice rezultate mai bune în general la transplantul de ficat şi o mai bună funcţionare imunitară.
Cercetătorii au identificat o nouă cale de expresie genetică care se activează în urma ischemiei şi a stresului datorat oxigenului.
Această cale, numită splicing alternativ, este o adaptare pe care celulele o folosesc pentru a-şi spori diversitatea proteinelor în momente de pericol, inflamaţie şi leziuni.
Cercetătorii au arătat că, în momentul în care celula sesizează condiţiile de oxigen scăzut, HIF-1α începe să reglementeze factorul de splicing al ARN, Ptbp1 (proteina 1 de aderare la calea Polypyrimidine-tract din ARN), care, la rândul său, direcţionează splicingul genei CEACAM1, ceea ce duce la versiunea protectoare CEACAM1-S, reducând leziunile hepatice care însoţesc transplantul.
În plus, cercetătorii au folosit o moleculă numită DMOG în studiile pe animale pentru a stabiliza HIF-1α in vivo, în condiţii normale de oxigen, ceea ce a stimulat în mod eficient versiunea protectoare a CEACAM1-S, oferind astfel o dovadă de concept terapeutic pentru studii viitoare.
„Aceste rezultate sugerează că CEACAM1-S poate fi un potenţial marker al calităţii ficatului şi că eforturile de a-i creşte expresia ar putea avea beneficii terapeutice pentru transplant sau leziuni hepatice acute", scriu cercetătorii.
Următorii paşi vor consta în testarea perfuzării ţesuturilor din ficatul uman suboptimal, care au fost păstrate la rece timp îndelungat, în prezenţa unor molecule numite morfoline care modifică expresia genelor.
Multe sute de gene sunt probabil supuse unui splicing alternativ într-un efort de a gestiona stresul celular care însoţeşte transplantul hepatic, explică cercetătorii.
„Ipoteza noastră este că, dacă putem identifica toate modificările de splicing alternativ care au loc în urma stresului ischemic, putem începe să înţelegem cu adevărat cum să 'întinerim' organele donatorilor, care joacă un rol important în reducerea penuriei de organe", a declarat Kenneth Dery, cercetător de proiect în cadrul departamentului de chirurgie al UCLA şi autorul principal al studiului.
„Formarea versiunii 'benefice' a CEACAM1-S înainte de transplantul de ficat are potenţialul de a acţiona ca un reglator al punctului de control al stresului legat de oxigen, observându-se o reducere a leziunilor de ischemie-reperfuzie hepatică", a precizat el.