Un laborator american a dezvoltat un algoritm inteligent cu ajutorul căruia cercetătorii au descoperit că multe medicamente neantibiotice, cum ar fi anumite antidepresive şi antiparazitare, au efecte antibacteriene şi ar putea ucide bacteriile rezistente la antibiotice.
Istoria omenirii s-a schimbat pentru totdeauna odată cu descoperirea antibioticelor în 1928. Bolile infecţioase precum pneumonia, tuberculoza şi septicemia erau răspândite şi letale până când penicilina le-a făcut tratabile.
Procedurile chirurgicale care odată veneau cu un risc ridicat de infecţie au devenit mai sigure şi mai de rutină. Antibioticele au marcat un moment triumfător al ştiinţei care a transformat practica medicală şi a salvat nenumărate vieţi.
Dar antibioticele au o avertizare inerentă: atunci când sunt folosite în exces, bacteriile pot dezvolta rezistenţă la aceste medicamente.
Organizaţia Mondială a Sănătăţii (OMS) a estimat că aceste superbacterii au provocat 1,27 milioane de decese în întreaga lume în 2019 şi vor deveni probabil o ameninţare tot mai mare la adresa sănătăţii publice globale în anii următori.
Noile descoperiri îi ajută pe oamenii de ştiinţă să facă faţă acestei provocări în moduri inovatoare.
Studiile au constatat că aproape un sfert dintre medicamentele care nu sunt prescrise în mod normal ca antibiotice, cum ar fi medicamentele utilizate pentru tratarea cancerului, a diabetului şi a depresiei, pot ucide bacteriile în doze prescrise în mod obişnuit pentru oameni.
Înţelegerea mecanismelor care stau la baza modului în care anumite medicamente sunt toxice pentru bacterii ar putea avea implicaţii de anvergură pentru medicină.
În cazul în care medicamentele neantibiotice ţintesc bacteriile în moduri diferite de cele ale antibioticelor standard, acestea ar putea servi drept piste pentru dezvoltarea de noi antibiotice.
Dar dacă medicamentele non-antibiotice ucid bacteriile în moduri similare cu antibioticele cunoscute, utilizarea lor prelungită, cum ar fi în tratamentul bolilor cronice, ar putea promova, fără să vrea, rezistenţa la antibiotice.
Într-o cercetare publicată recent în revista Science, oamenii de ştiinţă au dezvoltat o nouă metodă de învăţare automată care nu numai că a identificat modul în care non-antibioticele ucid bacteriile, dar poate ajuta, de asemenea, la găsirea de noi ţinte bacteriene pentru antibiotice.
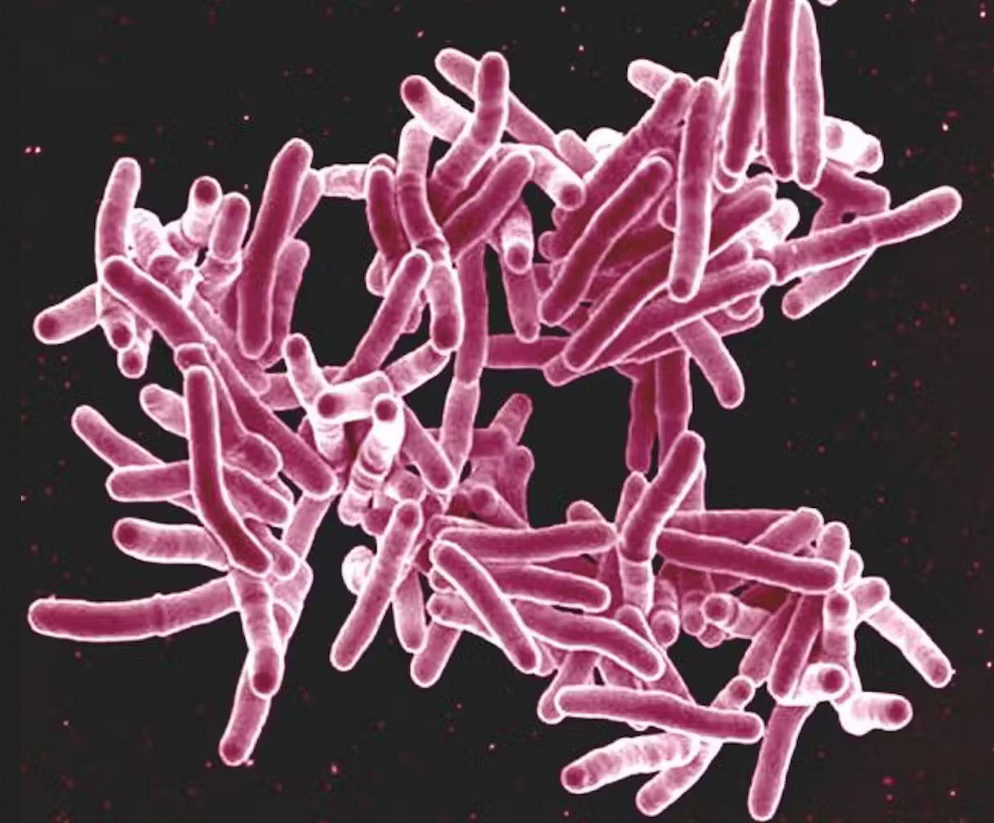 Imagine microscopică a unui grup de bacterii în formă de tijă colorate în roz. Mycobacterium tuberculosis este una dintre numeroasele specii microbiene care au dezvoltat rezistenţă la mai multe antibiotice. (NIAID/Flickr, CC BY)
Imagine microscopică a unui grup de bacterii în formă de tijă colorate în roz. Mycobacterium tuberculosis este una dintre numeroasele specii microbiene care au dezvoltat rezistenţă la mai multe antibiotice. (NIAID/Flickr, CC BY)
Noi modalităţi de a ucide bacteriile
Numeroşi oameni de ştiinţă şi medici din întreaga lume abordează problema rezistenţei la medicamente. Printre aceştia se numără şi cercetătorii care lucrează în laboratorul de la facultatea de medicină a UMass Chan.
Aceştia folosesc genetica patogenilor pentru a studia ce mutaţii fac bacteriile mai rezistente sau mai sensibile la medicamente.
După ce au aflat despre activitatea antibacteriană larg răspândită a neantibioticelor, echipa şi-a propus să descopere cum ucid bacteriile aceste medicamente.
Laboratorul a folosit o tehnică de screening genetic pe care au dezvoltat-o recent, pentru a studia modul în care medicamentele anticancerigene ţintesc bacteriile.
Această metodă identifică ce gene specifice şi ce procese celulare se modifică atunci când bacteriile suferă mutaţii.
Monitorizarea modului în care aceste modificări influenţează supravieţuirea bacteriilor permite cercetătorilor să deducă mecanismele pe care aceste medicamente le folosesc pentru a ucide bacteriile.
Laboratorul a colectat şi analizat aproape 2 milioane de cazuri de toxicitate între 200 de medicamente şi mii de bacterii mutante.
Folosind un algoritm de învăţare automată pe care l-au dezvoltat pentru a deduce similitudinile dintre diferite medicamente, oamenii de ştiinţă au grupat medicamentele pe baza modului în care acestea au afectat bacteriile mutante.
Hărţile au arătat în mod clar că antibioticele cunoscute au fost strâns grupate în funcţie de clasele lor cunoscute de mecanisme de distrugere.
De exemplu, toate antibioticele care vizează peretele celular - stratul gros de protecţie care înconjoară celulele bacteriene - au fost grupate împreună şi bine separate de antibioticele care interferează cu replicarea ADN-ului bacteriei.
În mod intrigant, atunci când echipa a adăugat medicamente neantibiotice la această analiză, cercetătorii au descoperit că acestea au format grupuri separate de antibiotice.
Acest lucru indică faptul că medicamentele non-antibiotice şi cele antibiotice au moduri diferite de a ucide celulele bacteriene.
În timp ce aceste grupări nu dezvăluie modul în care fiecare medicament ucide în mod specific antibioticele, ele arată că cele grupate împreună lucrează probabil în moduri similare.
Echipa şi-a propus să identifice noi ţinte de medicamente în bacterii pentru a le ucide.
Cercetătorii au cultivat sute de generaţii de bacterii care au fost expuse la diferite medicamente neantibiotice prescrise în mod normal pentru tratarea anxietăţii, a infecţiilor cu paraziţi şi a cancerului.
Secvenţierea genomurilor bacteriilor care au evoluat şi s-au adaptat la prezenţa acestor medicamente le-a permis să identifice proteina bacteriană specifică pe care triclabendazolul - un medicament utilizat pentru tratarea infecţiilor parazitare - o vizează pentru a ucide bacteriile.
Este important de subliniat faptul că antibioticele actuale nu ţintesc în mod obişnuit această proteină.
În plus, laboratorul a descoperit că alte două non-antibiotice care au folosit un mecanism similar cu cel al triclabendazolului ţintesc, de asemenea, aceeaşi proteină.
Acest lucru a validat algoritmul care a creat hărţile de similaritate a medicamentelor, pentru a le identifica pe cele cu mecanisme de ucidere similare, chiar şi atunci când mecanismul respectiv era încă necunoscut.
Contribuţia la descoperirea antibioticelor
Descoperirile deschid multiple oportunităţi pentru cercetători de a studia modul în care medicamentele neantibiotice acţionează diferit faţă de antibioticele standard.
Metoda de cartografiere şi testare a medicamentelor folosită de laboratorul UMass Chan are, de asemenea, potenţialul de a rezolva un blocaj critic în dezvoltarea antibioticelor.
Căutarea de noi antibiotice implică, de obicei, alocarea unor resurse considerabile pentru a examina mii de substanţe chimice care ucid bacteriile şi pentru a afla cum funcţionează. Se constată că majoritatea acestor substanţe chimice funcţionează în mod similar cu antibioticele existente şi sunt aruncate.
Noua cercetare arată că, prin combinarea screening-ului genetic cu învăţarea automată se poate ajunge la descoperirea mecanismului care poate ucide bacteriile în moduri pe care cercetătorii nu le-au folosit până acum.
„Există diferite modalităţi de a ucide bacteriile pe care nu le-am exploatat încă şi există şi alte direcţii pe care le putem urma pentru a combate ameninţarea infecţiilor bacteriene şi a rezistenţei la antibiotice", au concluzionat autorii în articolul publicat marţi, care descrie aceste descoperiri.