O echipă de medici britanici a eliminat cancerul incurabil al unei fetiţe de 13 ani, bolnavă de leucemie, utilizând, în premieră, un tratament revoluţionar. Cazul a fost prezentat de cercetători la reuniunea anuală a Societăţii Americane de Hematologie, care a avut loc în acest weekend, în New Orleans, Statele Unite.
Alyssa, o tânără adolescentă în vârstă de 13 ani, din Leicester, Marea Britanie, a fost diagnosticată cu leucemie limfoblastică acută cu celule T (T-ALL) în 2021. Fetiţa a fost tratată cu toate terapiile convenţionale existente pentru leucemia de care suferea, inclusiv chimioterapie şi transplant de măduvă osoasă, dar, din păcate, boala ei a recidivat şi pentru ea nu mai existau alte opţiuni de tratament.
Ea a devenit prima pacientă înscrisă în studiul clinic TvT şi, în mai 2022, a fost internată la unitatea de transplant de măduvă osoasă (BMT) de la GOSH, pentru a primi celule modificate genetic (CAR T „universale”) de la un donator voluntar sănătos.
Aceste celule au fost proiectate genetic după o nouă tehnologie inventată în urmă cu 6 ani, denumită ‘editarea bazei’ (editarea bazelor azotate din ADN), proiectată şi dezvoltată de aceeaşi echipă de cercetători de la University College London (UCL), condusă de profesorul Waseem Qasim de la spitalul de pediatrie Great Ormond Street (UCL GOS ICH).
Fără acest tratament experimental, singura opţiune a fetiţei era îngrijirea paliativă. „În cele din urmă aş fi murit”, a spus Alyssa.
Organismul fetiţei a fost pregătit cu receptori de antigen himeric (CAR) pentru a permite celulelor T vânarea şi distrugerea celulelor T canceroase, fără ca acestea să se atace şi să se distrugă între ele.
După doar 28 de zile, Alyssa a intrat în remisie şi a putut să primească un al doilea transplant de măduvă osoasă pentru a i se reface sistemul imunitar.
În prezent, la şase luni după transplant, adolescenta se simte bine şi este acasă, unde se recuperează alături de familia ei şi continuă monitorizarea post-transplant.
Deşi cancerul este în prezent nedetectabil, Alyssa este încă monitorizată pentru cazul în care boala ar recidiva.
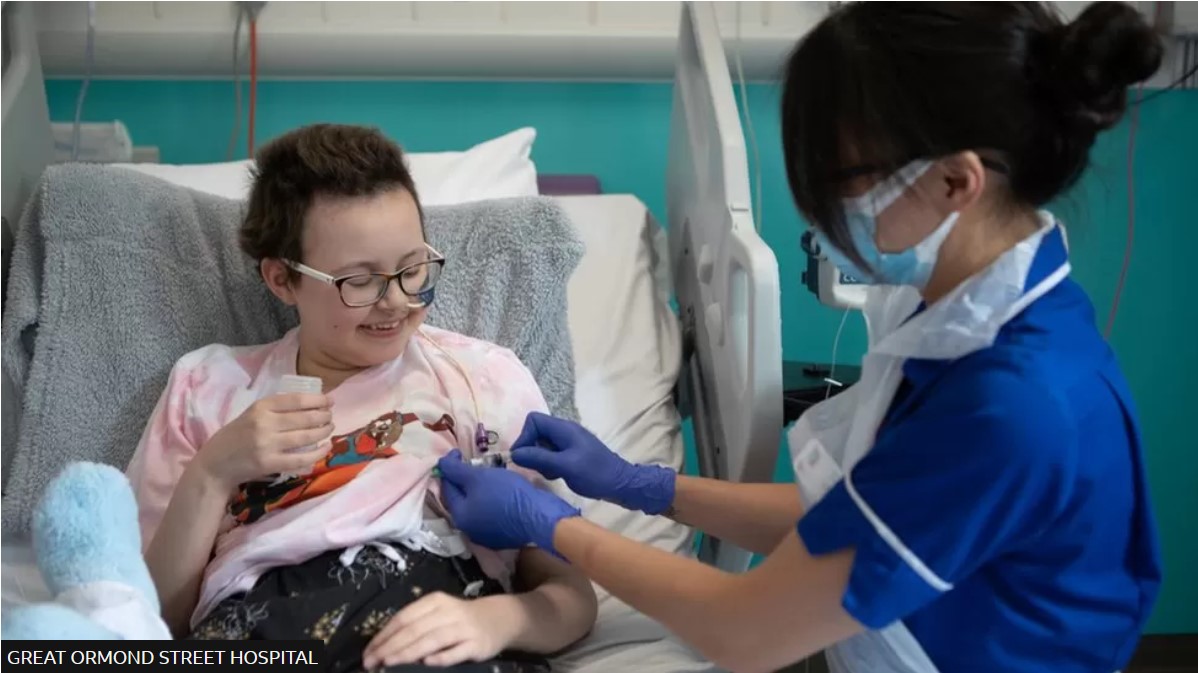 (foto: asistentă medicală de la spitalul Great Ormond Street, îi administrează Alyssiei terapia, în mai 2022)
(foto: asistentă medicală de la spitalul Great Ormond Street, îi administrează Alyssiei terapia, în mai 2022)
Cercetătorii au prezentat datele, în premieră, la reuniunea anuală a Societăţii Americane de Hematologie, care a avut loc în acest weekend, la New Orleans, în SUA.
Bazele chimice sunt limbajul vieţii. Cele patru baze azotate din ADN, adenina (A), citozina (C), guanina (G) şi timina (T) - în ARN timina este înlocuită de uracil - sunt elementele de bază ale codului genetic uman. Aşa cum literele din alfabet scriu cuvinte care au sens, miliardele de baz chimice din ADN-ul uman descriu manualul de instrucţiuni pentru funcţionarea organismului.
Editarea bazelor le permite oamenilor de ştiinţă să se concentreze pe o anumită porţiune din codului genetic şi să modifice structura moleculară a unei singure baze, transformând-o în alta, schimbând astfel instrucţiunile genetice.
Echipa mare de medici şi oameni de ştiinţă a folosit acest instrument pentru a proiecta un nou tip de celulă T, capabilă să vâneze şi să omoare celulele T canceroase ale pacientei.
Ei au prelevat celule T sănătoase de la un donator sănătos pe care le-au modificat astfel:
- O primă modificare în editarea bazei a fost dezactivarea mecanismului de ţintire al celulelor T, astfel încât acestea să nu atace organismul fetiţei
- A doua modificare a eliminat un marcaj chimic, numit CD7, care se află pe toate celulele T
- A treia modificare a fost crearea unei ‘mantii de invizibilitate’ pentru a împiedica distrugerea celulelor T modificate de către un medicament de chimioterapie, respectiv eliminarea unui al doilea „marcaj” numit CD52. Acest lucru face ca celulele editate să fie invizibile pentru unele dintre medicamentele puternice administrate pacientului în timpul tratamentului
- Etapa finală a constat în adăugarea unui receptor de antigen himeric (CAR) care recunoaşte receptorul celulelor T CD7 de pe celulele T leucemice, şi instruieşte celulele T să vâneze celulele cu marcajul CD7, astfel încât acestea să distrugă fiecare celulă T din corpul pacientei - inclusiv pe cele canceroase. Celulele devin armate împotriva CD7 şi recunosc şi luptă cu leucemia cu celule T. De aceea a fost nevoie ca acest marcaj să fie eliminat de pe celulele T folosite în terapie, pentru ca acestea să nu se distrugă între ele.
Aceste modificări au fost realizate prin „editarea bazei” - conversia chimică a bazelor unice nucleotidice (litere ale codului ADN) care poartă instrucţiuni pentru o anumită proteină.
De exemplu, schimbarea bazelor nucleotidice specifice din gena pentru CD7 de la o citozină la o timină creează un „codon stop” - echivalentul unui punct complet genetic - care împiedică maşina celulară să citească instrucţiunile complete şi producţia de CD7 este oprită.
În cazul în care terapia funcţiona, experţii aveau să reconstruiască sistemul imunitar al fetiţei, inclusiv celulele T, prin cel de-al doilea transplant de măduvă osoasă.
De când Alyssa s-a îmbolnăvit de leucemie în mai anul trecut, nu a obţinut niciodată o remisie completă. Nici cu chimioterapie, şi nici după primul transplant de măduvă osoasă. Abia după ce a primit terapia cu celule CD7 CAR-T şi un al doilea transplant de măduvă osoasă a scăpat de leucemie, spun medicii care o îngrijesc.

Tratamentele anterioare s-au bazat pe tehnici numite TALENS sau CRISPR/Cas9 pentru a aduce modificări genelor prin „tăieturi" (editări genetice) realizate cu „foarfeci” moleculari.
Noua abordare de editare a bazei chimice acţionează fără a provoca rupturi în ADN şi permite mai multe editări, cu mai puţine riscuri şi efecte nedorite asupra cromozomilor.
Tehnica este, de asemenea, investigată pentru a încerca să corecteze modificările dăunătoare ale codului ADN pentru o varietate de afecţiuni moştenite (ereditare).
În terapia Alyssei, fiecare dintre modificările editării bazei chimice a implicat „ruperea" unei secţiuni a codului genetic, astfel încât acesta să nu mai funcţioneze.
Dar există aplicaţii mai nuanţate în care, în loc să fie dezactivate anumite instrucţiuni, s-ar putea repara cea defectă. Anemia falciformă (siclemia sau drepanocitoza), de exemplu, este cauzată de o singură modificare a bazei care ar putea fi corectată.
În prezent există deja în curs de desfăşurare studii de editare a bazelor în boala celulelor seceră, precum şi în cazul colesterolului mare moştenit genetic şi tulburarea de sânge beta-talasemie.
„Am proiectat şi dezvoltat tratamentul de la laborator la clinică şi acum îl testăm pe copii din toată Marea Britanie, într-o abordare unică", a spus profesorul Waseem Qasim, profesor de terapie celulară şi genică la UCL GOS ICH.
„Povestea Alyssei este o mare demonstraţie a modului în care, cu echipe de experţi şi infrastructură, putem conecta tehnologiile de ultimă oră de laborator cu rezultate reale în spital pentru pacienţi. Este cea mai sofisticată inginerie celulară a noastră de până acum şi deschide calea pentru alte tratamente noi şi, în cele din urmă, pentru a oferi un viitor mai bun copiilor bolnavi", a spus medicul.
Studiul clinic pentru acest tratament este în prezent deschis şi îşi propune să recruteze până la zece pacienţi cu leucemie cu celule T care au epuizat toate opţiunile de tratament convenţionale.
Dacă se dovedeşte că va avea succes pe scară largă, echipele de transplant de măduvă osoasă şi de terapie cu celule CAR T de la GOSH speră că vor putea oferi mai devreme tratamentul copiilor, atunci când aceştia sunt mai puţin bolnavi, şi anticipează aplicaţii suplimentare pentru alte tipuri de leucemie în 2023.





