O echipă de oameni de ştiinţă sud-coreeni a făcut o descoperire care ar putea revoluţiona atât diagnosticul, cât şi tratamentul bolii Alzheimer. Grupul a identificat un mecanism prin care astrocitele din creier absorb niveluri ridicate de acetaţi, ceea ce le transformă în astrocite reactive periculoase. Oamenii de ştiinţă sud-coreeni au dezvoltat şi o nouă tehnică de imagistică care profită de acest mecanism pentru a observa direct interacţiunile dintre astrocite şi neuroni.
Se ştie că boala Alzheimer, una dintre principalele cauze ale demenţei, este asociată cu neuroinflamaţia în creier. În timp ce neuroştiinţa tradiţională a crezut mult timp că plăcile de beta-amiloid sunt cauza, tratamentele care vizează aceste plăci au avut puţin succes în tratarea sau încetinirea progresiei bolii Alzheimer.
Pe de altă parte, există şi alte teorii, printre care una, mai nouă, susţine că astrocitele reactive sunt adevăraţii vinovaţi din spatele bolii Alzheimer.
Astroglioza reactivă, un semn distinctiv al neuroinflamaţiei în maladia Alzheimer, precede adesea degenerarea sau moartea neuronală.
Echipa de cercetare condusă de directorul C. Justin Lee, de la Centrul pentru cogniţie şi sociabilitate din cadrul Institutului pentru Ştiinţe de Bază, din Coreea de Sud, a raportat anterior că astrocitele reactive şi enzima monoaminooxidază B (MAO-B) din aceste celule pot fi utilizate ca ţinte terapeutice pentru Alzheimer.
De asemenea, cercetătorii au confirmat existenţa unui ciclu al ureei în astrocite şi au demonstrat că ciclul activat al ureei promovează demenţa.
Cu toate acestea, în ciuda importanţei clinice a astrocitelor reactive, nu au fost încă dezvoltate sonde de neuroimagistică cerebrală care să poată observa şi diagnostica aceste celule la nivel clinic.
În această ultimă cercetare, echipa lui Lee a folosit imagistica prin tomografie cu emisie de pozitroni (PET) cu sonde radioactive (trasori) de acetat şi glucoză (11C-acetat şi 18F-FDG) pentru a vizualiza modificările metabolismului neuronal al pacienţilor cu Alzheimer.
„Acest studiu demonstrează o valoare academică şi clinică semnificativă prin vizualizarea directă a astrocitelor reactive, care au fost recent evidenţiate ca fiind o cauză principală pentru Alzheimer", a declarat dr. Nam Min-Ho, unul dintre primii autori ai acestei lucrări.
Mai mult, cercetătorii au demonstrat că acetatul, principalul component al oţetului, este responsabil pentru promovarea astrogliilor reactive, care induc producţia de putrezină şi GABA şi duc la demenţă.
În primul rând, cercetătorii au demonstrat că astrocitele reactive absorb excesiv de mult acetat prin intermediul unui transportor monocarboxilat-1 (MCT1) la niveluri ridicate în modelele de rozătoare cu astroglioză reactivă şi Alzhemer.
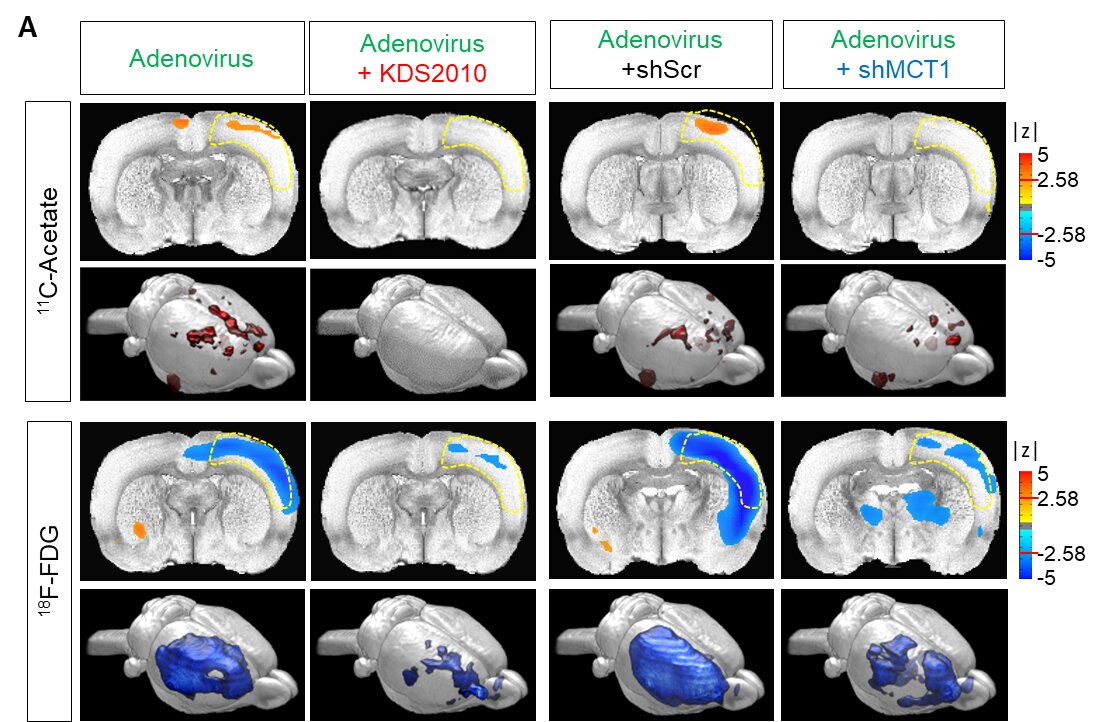
(Foto: Fig 1. Imagistica micro-PET in vivo cu 11C-acetat şi 18F-FDG in vivo în modelul cu adenovirus (model de astroglioză reactivă). A. Stânga, imagini parametrice dintr-o comparaţie bazată pe voxeli a imagisticii PET cu 11C-acetat şi 18F-FDG în modelul cu adenovirus cu sau fără tratament cu KDS2010. Dreapta, imagini parametrice din comparaţia bazată pe voxel a imagisticii 11C-acetat şi 18F-FDG PET în modelul adenovirus cu ARN-sh sau MCT1-ARN-sh. Credit: Institutul pentru Ştiinţe de Bază)
S-a descoperit că absorbţia crescută de acetat este asociată cu astroglioza reactivă şi stimulează sinteza aberantă de GABA astrocitară atunci când este prezentă amiloid-beta, o proteină toxică bine cunoscută în Alzheimer.
Cercetătorii au arătat că imagistica PET cu 11C-acetat şi 18F-FDG poate fi utilizată pentru a vizualiza hipermetabolismul acetatului indus de astrocitele reactive şi hipometabolismul asociat al glucozei neuronale în creierele cu neuroinflamare şi AD (Figura 1A).
Mai mult, atunci când cercetătorii au inhibat astroglioza reactivă şi expresia astrocitară MCT1 în modelul de şoarece cu Alzheimer, au reuşit să inverseze aceste modificări metabolice.
 (Foto: Fig. 2. Imagistica cu 11C-acetat şi 18F-FDG pentru vizualizarea astrogliozei reactive şi a hipometabolismului neuronal asociat al glucozei în creierul pacienţilor cu Alzheimer. A. Imagini PET reprezentative ale 11C-acetatului şi 18F-FDG la pacienţii cu Alzheimer şi la pacienţii de control. B. Corelaţii multiple între 11C-acetat SUVR, 18F-FDG SUVR în cortexul entorinal şi hipocampus şi scorurile MMSE - Examinarea minimă a stării mentale este un test cognitiv utilizat frecvent. Credit: Institutul pentru Ştiinţe de Bază).
(Foto: Fig. 2. Imagistica cu 11C-acetat şi 18F-FDG pentru vizualizarea astrogliozei reactive şi a hipometabolismului neuronal asociat al glucozei în creierul pacienţilor cu Alzheimer. A. Imagini PET reprezentative ale 11C-acetatului şi 18F-FDG la pacienţii cu Alzheimer şi la pacienţii de control. B. Corelaţii multiple între 11C-acetat SUVR, 18F-FDG SUVR în cortexul entorinal şi hipocampus şi scorurile MMSE - Examinarea minimă a stării mentale este un test cognitiv utilizat frecvent. Credit: Institutul pentru Ştiinţe de Bază).
„Astrocitele reactive au prezentat anomalii metabolice şi au absorbit excesiv de mult acetat în comparaţie cu starea normală. Am descoperit că acetatul joacă un rol important în promovarea răspunsurilor inflamatorii ale astrocitelor", a comentat dr. Yun Mijin.
Utilizând această nouă strategie de imagistică, grupul sud-coreean a descoperit că alterările metabolismului acetatului şi glucozei au fost observate în mod constant în modelul de şoarece cu Alzheimer şi la pacienţii umani cu Alzheimer (Figura 3A).
Ei au reuşit să confirme că există o corelaţie puternică între funcţia cognitivă a pacientului şi semnalele PET cu 11C-acetat şi 18F-FDG (Figura 3B).
Aceste rezultate sugerează că acetatul, considerat anterior o sursă de energie specifică astrocitelor, poate facilita astroglioza reactivă şi poate contribui la suprimarea metabolismului neuronal.
„Prin demonstrarea faptului că acetatul nu acţionează doar ca sursă de energie pentru astrocite, ci facilitează şi astroglioza reactivă, am sugerat un nou mecanism care induce astroglioza reactivă în bolile cerebrale", a precizat dr. Ryu Hoon.
Până în prezent, acumulările de proteine beta-amiloid (βA) au fost suspectate ca fiind principala cauză a Alzheimer şi, prin urmare, au fost principalul obiectiv al majorităţii cercetărilor în domeniul demenţei.
Imagistica PET care vizează aglomerările beta-amiloid a avut limitări în diagnosticarea pacienţilor, iar medicamentele menite să le elimine ca ţintă pentru tratamentul Alzheimer au eşuat toate până acum, spun experţii.
Potrivit acestora, noul studiu oferă o nouă posibilitate şi anume aceea de a utiliza imagistica PET cu 11C-acetat şi 18F-FDG pentru diagnosticarea timpurie a maladiei Alzheimer.
În plus, mecanismul recent descoperit al astrogliozei reactive prin intermediul acetatului şi al transportatorului MCT1 sugerează o nouă ţintă pentru tratamentul bolii Alzheimer.
„Am confirmat o recuperare semnificativă atunci când am inhibat MCT1, transportul de acetat specific astrocitelor, într-un model animal de Alzheimer. Ne aşteptăm ca MCT1 să poată fi o nouă ţintă terapeutică pentru maladia Alzheimer", a concluzionat dr. C. Justin Lee.





