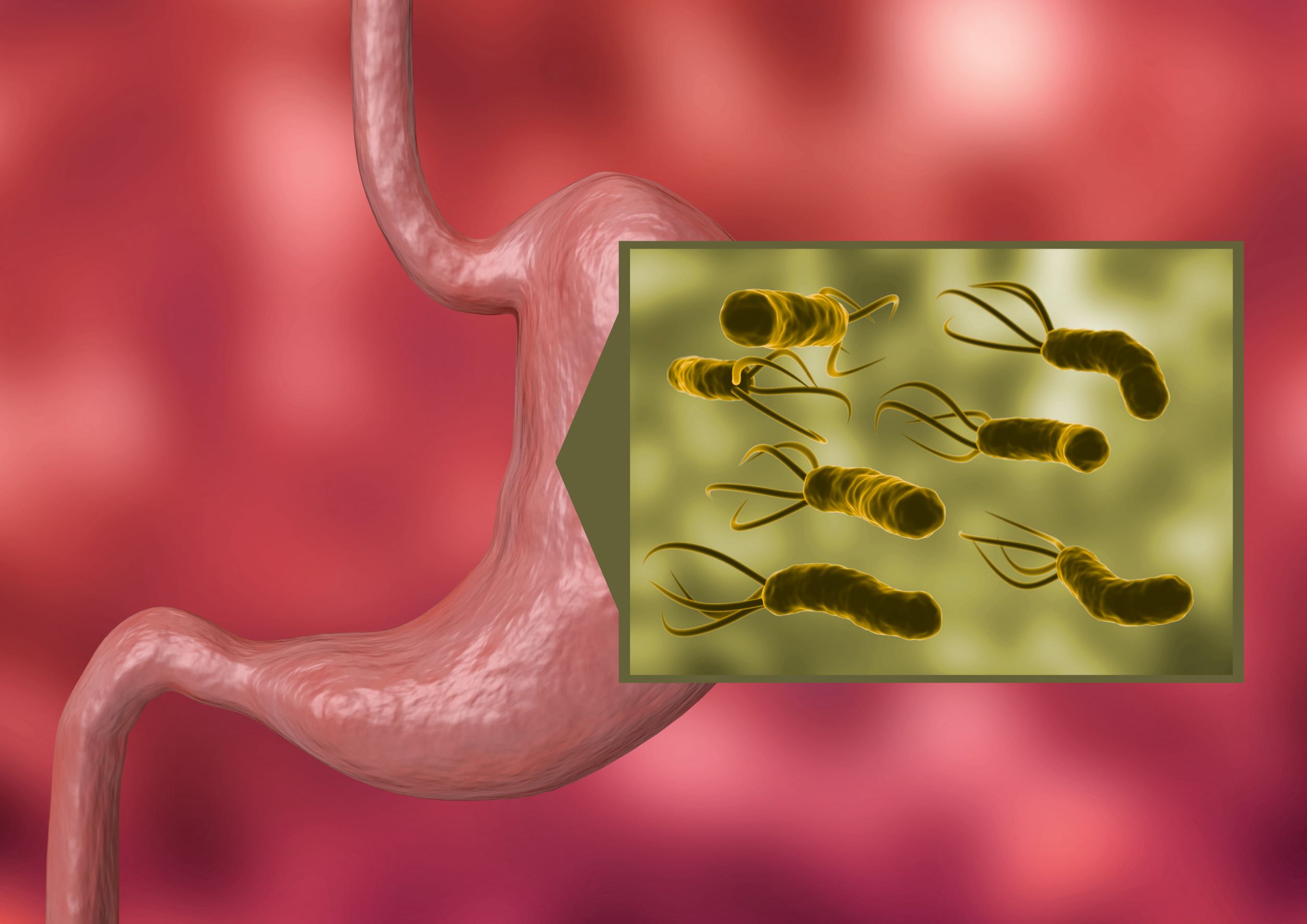
Cancerul de stomac este a patra cauză principală de deces prin cancer la nivel mondial şi are atât factori de risc de mediu, cât şi genetici. Din punct de vedere al mediului, infecţia cu Helicobacter pylori (H. pylori) creşte riscul de cancer de stomac, arată cercetătorii într-un recent studiu.
Întrucât virulenţa H. pylori în Asia de Est este ridicată, incidenţa cancerului de stomac este mai mare în ţări precum Japonia.
Din punct de vedere genetic, deşi variaţia genetică ereditară este motivul pentru care avem ochi de culori diferite şi suntem unici ca indivizi, uneori variantele genetice sunt asociate cu riscul de boală.
De exemplu, persoanele care poartă o anumită variantă patogenă ereditară a genei CDH1 au un risc crescut de cancer gastric.
Un amplu studiu caz-control realizat de cercetători internaţionali de la Centrul RIKEN pentru Ştiinţe Medicale Integrative (IMS) din Japonia a descoperit că persoanele care poartă anumiţi factori genetici de risc pentru cancerul gastric (de stomac) prezintă un risc mult mai mare dacă au fost infectate şi cu bacteria H. pylori.
Studiul, publicat joi, în The New England Journal of Medicine, ar putea contribui la dezvoltarea unei medicini genomice adaptate pentru tratarea cancerului de stomac.
Testarea pentru depistarea prezenţei variantelor patogene este în prezent una dintre numeroasele măsuri luate pentru prevenirea cancerului, supravegherea şi selectarea tratamentului.
toate acestea, deoarece lipsesc studiile caz-control la scară largă şi deoarece cele care există nu au evaluat modul în care riscul de cancer gastric se modifică atunci când variantele patogene interacţionează cu factori de mediu precum H. pylori, rămâne neclar ce măsuri clinice reale pot fi luate.
Pentru a aborda această problemă, cercetătorii au evaluat, prin urmare, riscul de cancer gastric într-un amplu studiu caz-control efectuat pe japonezi, luând în considerare dacă aceştia erau purtători de variante patogene şi dacă fuseseră infectaţi cu H. pylori.
Folosind o metodă de analiză genomică dezvoltată iniţial la RIKEN, echipa comună condusă de Yukihide Momozawa de la RIKEN IMS şi Keitaro Matsuo de la Aichi Cancer Center a analizat mostre de ADN de la peste 11.000 de pacienţi cu cancer de stomac şi 44.000 de persoane fără cancer pentru 27 de gene asociate cu tumorile ereditare.
Analiza a identificat nouă gene care erau foarte asociate cu riscul de cancer de stomac.
În continuare, cercetătorii au analizat interacţiunea dintre variantele patogene din cele nouă gene şi istoricul pacienţilor cu infecţie cu H. pylori.
În primul rând, ei au descoperit că riscul de cancer gastric era dramatic mai mare atunci când o variantă patogenă era combinată cu infecţia cu H. pylori decât atunci când oricare dintre factori era prezent singur.
Dintre cele nouă gene, patru au prezentat un interes deosebit, deoarece codifică proteine care, în mod normal, ajută la repararea ADN-ului deteriorat.
Primul autor al studiului, Yoshiaki Usui, crede că aceste variante patogene exacerbează daunele provocate de infecţia cu H. pylori.
„Infecţia cu H. pylori duce la apariţia cancerului deoarece favorizează rupturile de dublu catenar al ADN-ului şi destabilizează ADN-ul celulelor stomacale", explică Usui.
Potrivit cercetătorului, combinarea infecţiei cu H. pylori cu variantele genetice care împiedică repararea normală a daunelor pare să sporească substanţial riscul de cancer gastric.
Deoarece prevalenţa infecţiei cu H. pylori este ridicată, iar eradicarea acesteia s-a dovedit dificilă, depistarea variantelor patogene poate ajuta la determinarea persoanelor care ar trebui să fie prioritare pentru intervenţii.
În general, reducerea riscului de cancer de stomac prin testarea infecţiei cu H. pylori şi eradicarea acesteia rămâne o prioritate ridicată pentru toată lumea, indiferent dacă sunt sau nu purtători ai variantelor patogene.
„Pentru practica clinică, va trebui să determinăm în ce măsură eradicarea H. pylori are de fapt un efect preventiv sau când ar trebui luată în considerare eradicarea", spune Matsuo.
Acest studiu face parte dintr-un efort amplu de a dezvolta modalităţi mai bune de prevenire şi tratare a cancerului prin înţelegerea modului în care interacţionează factorii de mediu şi cei genetici.
„Informaţiile obţinute în urma studiului vor contribui la ghidurile de practică medicală privind cancerul gastric şi variantele patogene şi se aşteaptă să contribuie la stabilirea unui sistem de medicină genomică personalizat, inclusiv la îmbunătăţirea acurateţei diagnosticului, la dezvoltarea de terapii care vizează genele cauzatoare şi la măsuri preventive mai adecvate pentru cancerul gastric", spune Momozawa.