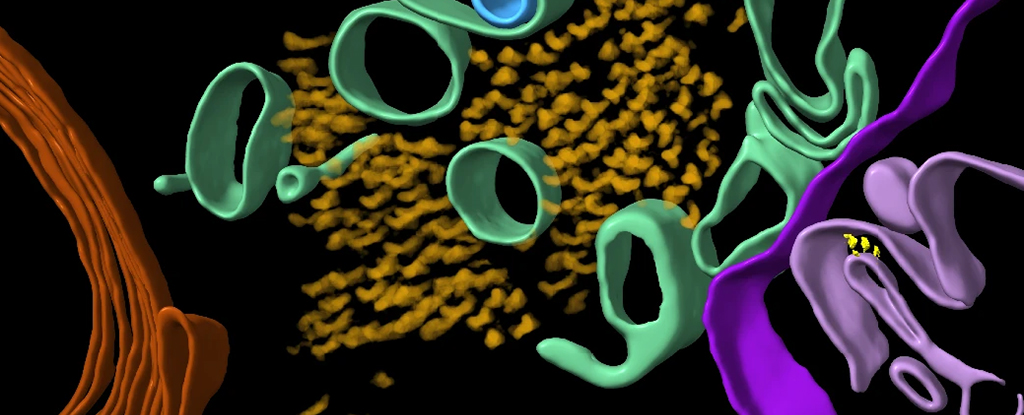
Un nou studiu a dezvăluit pentru prima dată structura moleculară a creierului afectat de boala Alzheimer. Cercetătorii au produs modele 3D de proteine din creier, inclusiv două proteine care sunt asociate, în mod special cu boala Alzheimer: beta-amiloid şi tau.
Oamenii de ştiinţă continuă să lucreze la tratamente pentru boala neurodegenerativă, şi pentru asta este important ca să înţeleagă cât mai multe despre această maladie.
Grupurile de proteine beta-amiloid şi tau din creier sunt fie o cauză a bolii Alzheimer, fie o consecinţă a acesteia - nu este încă foarte clar care dintre aceste variante.
O echipă de la Universitatea Leeds, din Marea Britanie, a reuşit să obţină imagini a modului în care aceste aglomerări sunt dispuse, până la cele mai mici detalii microscopice.
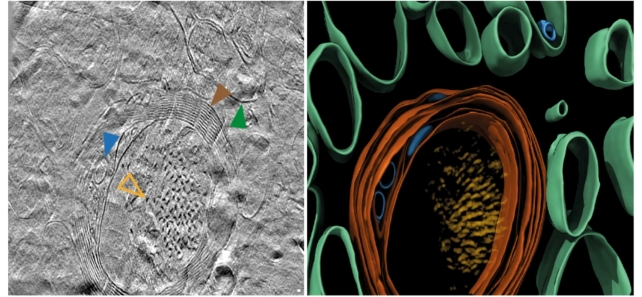
Stânga: Secţiune tomografiată a patologiei tau intracelulare în creierul Alzheimer postmortem. Dreapta: Culorizare pentru îmbunătăţirea imaginii, pentru a evidenţia moleculele. Portocaliu = filament tau; maro = axon mielinizat; verde = compartiment subcelular; albastru = organel intracelular legat de membrană. (Gilbert et al., Nature, 2024)
„Această primă privire asupra structurii moleculelor din interiorul creierului uman afectat oferă indicii suplimentare cu privire la ceea ce se întâmplă cu proteinele în boala Alzheimer", spune neurologul René Frank de la Universitatea din Leeds, într-un comunicat.
„Stabileşte, de asemenea, o abordare experimentală care poate fi aplicată pentru a înţelege mai bine o gamă largă de alte boli neurologice devastatoare", precizează medicul specialist.
Cercetătorii au utilizat o serie de tehnici avansate de imagistică pentru a scana ţesutul cerebral postmortem de la pacienţii cu Alzheimer, inclusiv tomografia crioelectronică (crioET) - care utilizează citirile din fasciculele de electroni pentru a cartografia structurile 3D ale ţesuturilor imobilizate la temperaturi foarte scăzute.
CryoET permite imagistica fără ca fixarea chimică sau deshidratarea să perturbe structura ţesutului biologic, ceea ce înseamnă că oamenii de ştiinţă pot acum să reconstruiască volume 3D de ţesut la rezoluţii de un milion de ori mai mici decât un bob de orez.
„Caracterizarea la microscopul optic a amiloidului în creierul bolnavului de Alzheimer a constituit baza diagnosticului şi a clasificării bolii", scriu cercetătorii în lucrarea publicată.
„Structura in situ a amiloidului în creierul uman este necunoscută".
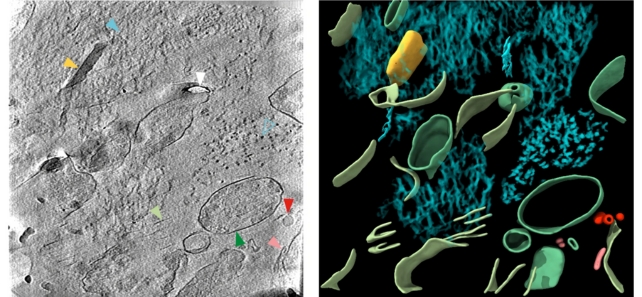
Felie tomografiată a patologiei β-amiloide în creierul bolnavului de Alzheimer postmortem. Dreapta: Imagine îmbunătăţită princolorizare pentru a indica moleculele. Cyan = fibrile; galben = particulă extracelulară cuboidală; roşu = picătură extracelulară; roz = veziculă extracelulară; verde închis = compartiment subcelular; verde deschis = compartiment al membranei plasmatice sparte. (Gilbert et al., Nature, 2024)
Prin observarea atât de detaliată a acestor proteine, se speră că va fi mai bine înţeles cum se formează aglomerările şi cum afectează creierul.
În cazul proteinelor beta-amiloide, a fost identificat un amestec de structuri microscopice asemănătoare firelor, numite fibrile, şi alte structuri.
În cazul proteinelor tau, au fost identificate aglomerări de filamente în linii drepte, deşi aranjamentul pare să varieze în funcţie de locul în care se află proteinele în creier.
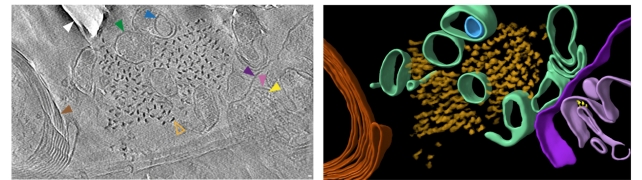
Stânga: Felie tomografiată a patologiei tau extracelulare în creierul bolnavului de Alzheimer postmortem. Dreapta: Culorizare pentru a evidenţia moleculele. Portocaliu = filament tau; maro = axon mielinizat; violet închis şi violet deschis = membranele externă şi internă ale mitocondriilor deteriorate; galben = ATPază Fo-F1 putativă; închis = compartiment subcelular; albastru = organel intracelular legat de membrană. (Gilbert et al., Nature, 2024)
În timp ce grupurile erau similare între ele, existau diferenţe în organizarea spaţială, în ceea ce priveşte modul în care filamentele tau erau orientate şi răsucite, precum şi în dimensiunea fibrilelor beta-amiloide.
Este pentru prima oară când aceste proteine sunt observate la acest nivel de detaliu şi de aceea este prea devreme pentru a comenta semnificaţia acestora, spun specialiştii. Demonstrând acum că tehnica funcţionează, aceasta poate fi încercată pe ţesuturi provenite de la o gamă mai largă de donatori.
Acest lucru va dezvălui mai multe despre modul în care aceste diferite proteine arată în diferite momente ale evoluţiei bolii Alzheimer şi, prin compararea acestor structuri în timp, experţii ar trebui să poată vedea cum evoluează boala.
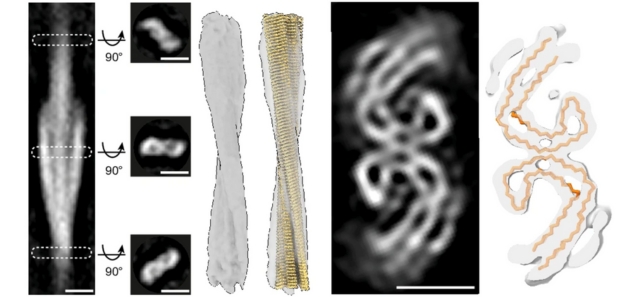
Cartografierea filamentelor tau din tomografii. În extrema stângă se află o vedere elicoidală a unei probe de filament tau. (Gilbert et al., Nature, 2024)
De fapt, echipa din spatele noului studiu crede că această abordare ar putea fi utilă în analiza cauzelor profunde ale tuturor tipurilor de boli neurodegenerative, aşa că ne putem aştepta să auzim mai multe despre ea în viitor.
„Cohorte mai mari de donatori diverşi cu boală Alzheimer, în diferite regiuni ale creierului şi în stadii mai timpurii ale bolii, pot dezvălui modul în care organizarea spaţială a amiloidului din diferite structuri se referă la profilurile neuropatologice individuale", scriu cercetătorii.
„Va fi, de asemenea, importantă aplicarea acestor abordări la alte afecţiuni neurodegenerative, dintre care multe împărtăşesc tipuri de neuropatologie amiloidă înrudite sau suprapuse".
Cercetarea a fost publicată recent în revista Nature.
Foto articol: Imagine îmbunătăţită prin colorizarea proteinelor tau scanate în creier. Credit: Gilbert et al., Nature, 2024.