Un parazit care este capabil să traverseze bariera hemato-encefalică pentru a infecta creierul gazdelor ar putea fi folosit, într-o zi, ca un mijloc de administrare a unor terapii pentru tratarea unor afecţiuni cerebrale majore.
Cercetătorii de la Universitatea Tel Aviv au modificat „parazitul pisicii", toxoplasma gondii, pentru a produce şi elibera proteine terapeutice în creierul uman.
Toxoplasma gondii - un parazit care prosperă în aproape toate vieţuitoarele cu sânge cald de pe Pământ - ar putea fi proiectat genetic pentru a furniza proteine terapeutice celulelor din creier, oferind opţiuni de tratament pentru afecţiuni greu accesibile.
Studiul a fost condus de profesorul Oded Rechavi de la Departamentul de Neurobiologie şi Şcoala Sagol de Neuroştiinţe de la Universitatea din Tel Aviv (UAT), împreună cu doctorandul, dr. Shahar Bracha, şi cu profesorul Lilach Sheiner, om de ştiinţă israelian şi expert în toxoplasmă de la Universitatea din Glasgow, Scoţia.
Rezultatele au fost publicate în principala revistă ştiinţifică Nature Microbiology.
„Una dintre cele mai mari provocări în tratarea bolilor neurologice este trecerea prin bariera hemato-encefalică (BHE)", explică prof. Rechavi într-un comunicat.
Este foarte dificil să se livreze medicamente la creier prin fluxul sanguin, iar acest lucru este valabil mai ales pentru moleculele mari, cum ar fi proteinele, 'maşinăriile' cheie care îndeplinesc multe funcţii importante în interiorul celulei.
Soluţia creativă propusă de echipa UAT utilizează parazitul unicelular Toxoplasma gondii, care poate infecta o mare varietate de organisme, dar se reproduce numai în intestinele pisicilor.
Parazitul este foarte eficient în infectarea oamenilor, aproximativ o treime din populaţia globală fiind infectată la un moment dat în viaţă.
Prof. Rechavi explică faptul că, „majoritatea oamenilor nici nu simt infecţia sau prezintă doar simptome uşoare asemănătoare gripei. Cu toate acestea, parazitul este periculos pentru persoanele cu insuficienţă imunitară cauzată de afecţiuni precum SIDA şi pentru fetuşii al căror sistem imunitar nu s-a dezvoltat încă. Acesta este motivul pentru care femeile însărcinate sunt sfătuite să nu mănânce carne crudă, care ar putea conţine parazitul, şi să stea departe de pisici, care l-ar putea transmite prin fecale".
În timp ce eliberează organismul de parazit, un sistem imunitar sănătos are doar un acces limitat la creier, iar parazitul rămâne în creier pe toată durata vieţii purtătorului.
Capacitatea parazitului de a pătrunde în creierul uman şi de a supravieţui acolo într-o stare latentă, fără să se reproducă, l-a făcut un candidat perfect pentru noua abordare a cercetătorilor: ingineria genetică a toxoplasma gondii pentru a secreta proteine terapeutice.
„Parazitul are trei sisteme de secreţie distincte, iar noi am experimentat pe două dintre ele", spune profesorul Rechavi.
„Nu am intervenit asupra primului sistem, care secretă proteine în afara neuronilor. Al doilea sistem 'lansează' un 'harpon' în neuron, pentru a permite pătrunderea. Odată intrat, parazitul formează un fel de chist în care continuă să secrete proteine în permanenţă. Am modificat ADN-ul parazitului pentru a-l face să producă şi să secrete proteinele dorite, care au potenţial terapeutic", a explicat cercetătorul
Capacitatea parazitului de a trece prin BHE şi de a comunica cu neuronii, combinată cu capacitatea noastră de a modifica genetic parazitul, generează o oportunitate de aur pentru rezolvarea marii provocări terapeutice de a livra medicamente la creier, spune profesorul Sheiner.
În acest studiu, echipa a folosit animale model transgenice cărora li s-au injectat paraziţi modificaţi genetic pentru a produce şi secreta proteine care ajung în nucleele celulelor.
Mai multe dovezi au demonstrat că proteinele au fost livrate în zona ţintă şi au rămas active în nucleele neuronilor.
Una dintre acestea a fost deosebit de atrăgătoare: o proteină care, livrată de parazit, a intrat în nuclee şi a tăiat segmente specifice de ADN, determinând creierul animalelor transgenice să strălucească în întuneric.
Această descoperire poate avea implicaţii de mare amploare pentru o serie de boli grave.
În studiul de faţă, cercetătorii au demonstrat în mod specific livrarea unei proteine numite MeCP2, a cărei deficienţă este asociată cu sindromul Rett.
„Acesta este un sindrom mortal cauzat de o deficienţă a unei singure gene numite MePC2 în celulele creierului, iar Toxoplasma gondii modificată de noi a fost capabilă să o livreze celulelor ţintă", spune prof. Rechavi. "
Dar acesta este doar un exemplu, menţionează cercetătorul.
Există multe alte boli cauzate de deficienţa sau expresia anormală a unei anumite proteine.
Pentru a asigura implementarea terapeutică sigură şi eficientă a metodei, atât pentru administrarea de medicamente, cât şi pentru editarea genetică, a fost înfiinţată o societate denumită Epeius, în colaborare cu Ramot - societatea de transfer tehnologic a Universităţii din Tel Aviv, şi cu serviciile de cercetare şi inovare ale Universităţii din Glasgow.
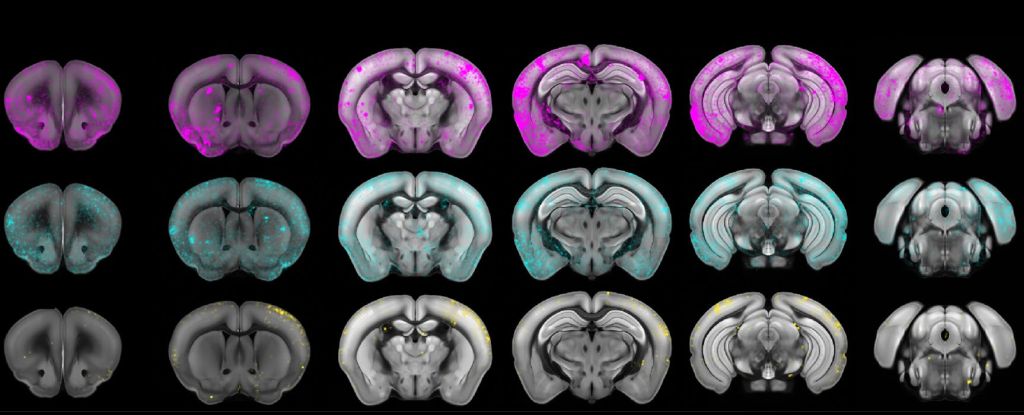
Foto: Creierul şoarecilor după injectarea cu T. gondii needitat (rândul de sus), T. gondii editat (mijloc) şi soluţie salină (jos). Credit: Bracha et al., Nat. Microbiol., iulie 2024.