Un nou studiu arată că un medicament utilizat pentru tratarea bolii Parkinson perturbă semnificativ microbiomul intestinal prin inducerea deficienţei de fier. Cercetătorii au utilizat tehnici avansate de imagistică şi moleculare pentru a arăta că medicamentul inhibă bacteriile benefice, promovând în acelaşi timp creşterea E. coli, care prosperă în condiţii de lipsă de fier.
Un studiu de referinţă arată că, entacapona, un medicament prescris pe scară largă pentru boala Parkinson, poate perturba semnificativ microbiomul intestinal prin provocarea unei deficienţe de fier.
Realizat de un grup internaţional de cercetători, de la Universitatea din Viena, în colaborare cu Universitatea din Southampton, Universitatea din Aalborg şi Universitatea din Boston, studiul a fost publicat în revista Nature Microbiology.
Această cercetare aruncă o lumină asupra modului în care medicamentele pot modifica neintenţionat comunităţile microbiene care joacă un rol important în sănătate.
Medicamentul împotriva bolii Parkinson modifică microbiomul intestinal
Deşi este bine cunoscut faptul că antibioticele pot perturba bacteriile intestinale, cercetările recente arată că multe alte medicamente - în special cele utilizate pentru tratarea tulburărilor neurologice - pot avea, de asemenea, un impact major. Deşi aceste medicamente sunt concepute pentru a viza organe specifice, ele pot perturba în mod neintenţionat echilibrul bacteriilor intestinale, putând duce la probleme de sănătate.
Până în prezent, majoritatea studiilor privind aceste interacţiuni medicament-microbiom s-au bazat pe datele pacienţilor afectate de variabile multiple sau pe experimente care foloseau bacterii izolate, care nu reuşesc să reflecte complexitatea microbiomului intestinal uman.
Acum, într-un nou studiu revoluţionar, realizat în cadrul Clusterului de excelenţă finanţat de Fondul Austriac pentru Ştiinţă (FWF) „Microbiomul conduce la sănătatea planetei/Microbiomes drive Planetary Health”, oamenii de ştiinţă de la Universitatea din Viena, în colaborare cu Universitatea din Southampton, Universitatea din Aalborg şi Universitatea din Boston, au arătat că entacapona, medicament prescris pe scară largă pentru boala Parkinson, perturbă semnificativ microbiomul intestinal uman prin inducerea unei deficienţe de fier.
O nouă concepţie de studiu pentru investigarea interacţiunilor medicament-bacterii
Folosind o nouă abordare experimentală, echipa internaţională a studiat efectele a două medicamente - entacapona şi loxapina, un medicament pentru schizofrenie - asupra probelor fecale de la donatori umani sănătoşi. Ei au incubat probele cu concentraţii terapeutice ale acestor medicamente şi apoi au analizat impactul asupra comunităţilor microbiene utilizând tehnici moleculare şi imagistice avansate, inclusiv marcarea cu apă grea combinată cu spectroscopia Raman stimulată (SRS).
Echipa a descoperit că loxapina şi mai ales entacapona au inhibat sever mulţi membri ai microbiomului, în timp ce E. coli s-a extins dramatic în prezenţa entacaponei.
„Rezultatele au fost şi mai izbitoare atunci când am examinat activitatea microbiană, nu doar abundenţa lor”, a explicat într-un comunicat Fatima Pereira, autor principal al studiului şi fost cercetător postdoctoral la Universitatea din Viena.
Metoda SRS cu apă grea le-a permis cercetătorilor să observe modificările subtile, dar semnificative ale microbiomului intestinal, care sunt adesea ratate în măsurătorile tradiţionale bazate pe abundenţă.
Entacapona induce carenţa de fier, favorizând microbii patogeni
Cercetătorii au emis ipoteza că entacapona ar putea interfera cu disponibilitatea fierului în intestin, o resursă cheie pentru mulţi microbi.
Experimentele lor au confirmat că adăugarea de fier la eşantioanele fecale care conţineau entacaponă a contracarat efectele medicamentului de modificare a microbiomului. Investigaţii suplimentare au arătat că E. coli, care prospera în aceste condiţii, avea un sistem foarte eficient de absorbţie a fierului (enterobactin siderophore). Acest sistem a permis bacteriei să depăşească deficienţa de fier şi să prolifereze, chiar şi în prezenţa medicamentului.
„Arătând că entacapona induce carenţa de fier, am descoperit un nou mecanism de disbioză intestinală indusă de medicamente, în care medicamentul selectează E. coli şi alţi microbi potenţial patogeni bine adaptaţi la condiţiile de limitare a fierului”, a declarat Michael Wagner, director ştiinţific al grupului de excelenţă şi director adjunct al Centrului pentru microbiologie şi ştiinţa sistemelor de mediu (CeMESS) de la Universitatea din Viena.
Implicaţii mai largi pentru interacţiunile medicament-microbiom
Această descoperire are implicaţii mai largi pentru înţelegerea modului în care alte medicamente destinate oamenilor ar putea afecta microbiomul intestinal. Mai multe medicamente, inclusiv entacapona, conţin grupe catecol care se leagă de metale, ceea ce sugerează că acest mecanism ar putea fi o cale mai comună pentru alterările microbiomului induse de medicamente.
Constatările prezintă, de asemenea, o oportunitate de a atenua efectele secundare ale medicamentelor precum entacapona. Prin asigurarea unei disponibilităţi suficiente de fier pentru intestinul gros, ar putea fi posibilă reducerea disbiozei şi a problemelor gastrointestinale care însoţesc adesea tratamentul bolii Parkinson.
„Următorul pas este să explorăm modul în care putem modifica tratamentele medicamentoase pentru a susţine mai bine microbiomul intestinal”, a spus Wagner. „Ne uităm la strategii de livrare selectivă a fierului în intestinul gros, unde poate aduce beneficii microbiomului fără a interfera cu absorbţia medicamentelor în intestinul subţire.”
Acest studiu a fost realizat ca parte a Clusterului de excelenţă finanţat de FWF „Microbiomes drive Planetary Health”, o iniţiativă de cercetare în colaborare care include opt instituţii de cercetare austriece de top.
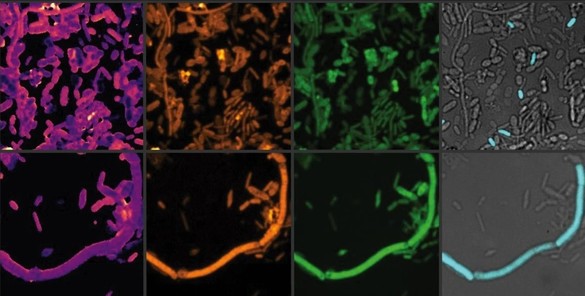
Imagistica chimică a microbilor intestinali activi. După o scurtă incubare cu apă grea, mediu de cultură şi un medicament, diferite legături chimice (aici C-D şi C-H) din proba de scaun sunt prezentate în galben şi verde, iar raportul lor în galben-violet (stânga). Microbii selectaţi sunt detectaţi în aceeaşi secţiune a imaginii cu sonde oligonucleotidice marcate cu fluorescenţă cyan. Activitatea microbilor detectaţi poate fi determinată pe baza cantităţii de legături C-D. Credit: Xiaowei Ge, Universitatea din Viena.





