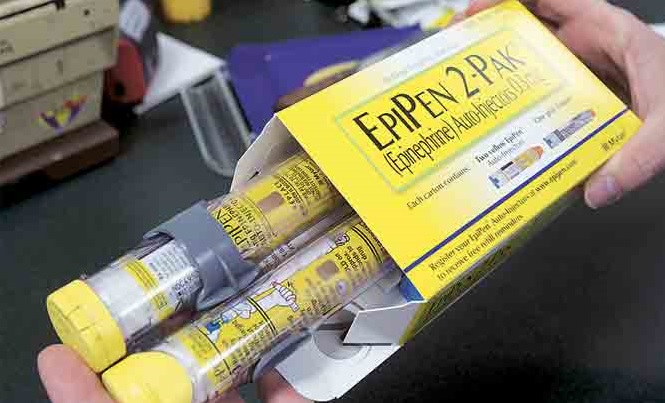
Autoritatea de reglementare în domeniul medicamentelor din Statele Unite (FDA) a aprobat joi prima versiune generică a medicamentului EpiPen pentru tratamentul de urgenţă al reacţiilor alergice severe (anafilaxie), produsă de compania farmaceutică israeliană Teva Pharmaceutical Industries, relatează Reuters.
EpiPen este o soluţie sterilă în stilou preumplut cu adrenalină (epinefrină) pentru injectarea de urgenţă în muşchi în caz de reacţii alergice severe (anafilaxie), cauzate de alergeni precum alimente, medicamente, înţepături sau muşcături de insecte sau induse de exerciţiul fizic sau de cauze necunoscute, potrivit autorizaţiei de punere pe piaţă aprobate de Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale (ANMDM) din România, consultată de 360medical.ro.
Soluţia EpiPen este produsă degrupul farmaceutic Mylan, care a lansat propria versiune generică a produsului în 2016.
FDA a aprobat între timp alte câteva soluţii injectabile cu adrenalină, precum Adrenaclick şi Auvi-Q, însă acestea nu sunt considerate copii ale EpiPen, astfel că soluţia produsă de Teva este prima versiune generică a medicamentului care concurează produsul original.
Producătorul Mylan a fost criticat dur în ultimul an în Statele Unite, după ce publicul a aflat că preţul EpiPen a crescut cu peste 400% în ultimul deceniu.
În plus, în ultimul an a existat o criză de aprovizionare cu EpiPen în America de Nord şi în Europa din cauza unor probleme legate de producţie, iar FDA a adăugat medicamentul pe lista produselor pentru care se înregistrează penurie pe piaţă.
"Această aprobare înseamnă că pacienţii cu alergii severe, care au nevoie de acces constant la epinefrina care le salvează viaţa, vor avea opţiuni mai ieftine, iar un nou produs aprobat înseamnă reducerea riscului de penurie", a afirmat Scott Gottlieb, comisar în cadrul FDA.
Mylan a cumpărat drepturile asupra EpiPen în 2007 şi a scumpit apoi rapid produsul.
Din această cauză, compania a fost acuzată că a majorat nejustificat costurile sistemului public de sănătate în Statele Unite, acceptând să plătească 465 milioane dolari în urma unui acord cu Departamentul Justiţiei din SUA.
Însă veniturile companiei din vânzările de EpiPen au scăzut puternic în ultimul an ca urmarea competiţiei tot mai mari şi a lansării propriei versiuni generice de către Mylan, mai ieftine.
Teva a încercat încă din 2016 să obţină aprobarea pentru versiunea generică a EpiPen, însă în primă fază a primit aviz negativ.
După anunţul FDA, acţiunile Teva, listate în SUA, s-a apreciat cu 6%, în timp ce acţiunile Mylan s-au ieftinit cu 1,3%.